
前回「消化液と消化酵素の違い」を勉強してきたよね。
実はね、
消化液と消化酵素の種類はたくさんある!
中学理科で勉強する種類一覧を表でまとめてみたよ。
| 消化酵素 | 消化液 | 分解するもの | 消化液が作られる場所 |
|---|---|---|---|
| アミラーゼ | だ液 | デンプン | だ液せん |
| ペプシン | 胃液 | タンパク質 | 胃 |
| トリプシン | すい液 | タンパク質 | すい臓 |
| リパーゼ | すい液 | 脂肪 | すい臓 |
うん、こりゃ、カタカナ多くて覚えづらいね。
ここではこの消化液と消化酵素の種類の覚え方を伝授するよ。
まずはだ液に含まれる「アミラーゼ」という消化酵素の覚え方。
この消化酵素はデンプンを分解する働きを持っているよ。
次の覚え方でどうだろう。
あかいミラーぜったい電車(でんしゃ)でプンプンだ駅(えき)
そう、なぜか赤色のミラーが電車の車内でプンプン怒っちゃってる駅、があるみたいなんだよね。

妖精の世界には。
次は胃液に含まれる消化酵素「ペプシン」の覚え方。
この消化酵素は、タンパク質を分解してアミノ酸に変える働きを持っているよ。
この覚え方でどうだろう。
ペースプリプリ信者(しんじゃ)淡白(たんぱく)でもいい駅(えき)
これも妖精の世界にある電車の駅だ。
マイペースなんだけど、プリプリしているある宗教の信者がいる。
その信者は、淡白でも良い、と認められている駅があるみたいなんだよね。

妖精の世界には。
次はすい液にある消化酵素「トリプシン」の覚え方だよ。
ペプシンと同じように、タンパク質を分解してアミノ酸に変える働きを持っているよ。
次の覚え方でもどうだろう。
トリケラトプス新登場(しんとうじょう)誕生(たんじょう)パッ
ク安(やす)い駅(えき)
恐竜のトリケラトプスが新しく登場、そして誕生するパックが売られていて、そのバックが安い駅があるみたいなんだよね。

妖精の世界には。
次はすい液に含まれる消化酵素「リパーゼ」の覚え方だよ。
脂肪を分解して「脂肪酸」と「モノグリセリド」に分解する働きを持っているんだ。
次の覚え方でどうだろう。
りかのパーマ贅沢(ぜいたく)志望者(しぼうしゃ)すいすい駅(えき)
これも妖精の世界にある駅の名前だね。
「りか」という女性のパーマは贅沢なんだけど、そのパーマにしたい志望者が多いんだって。
でもね、その志望者はなぜかスイスイ通れる駅があるようなんだよね、妖精の世界には。

うん、以上が中学理科で勉強する消化液と消化酵素の種類だよ。

| 消化酵素 | 消化液 | 分解するもの | 消化液が作られる場所 |
|---|---|---|---|
| アミラーゼ | だ液 | デンプン | だ液せん |
| ペプシン | 胃液 | タンパク質 | 胃 |
| トリプシン | すい液 | タンパク質 | すい臓 |
| リパーゼ | すい液 | 脂肪 | すい臓 |
次はだ液の実験で大活躍する「ベネジクト液とヨウ素液の違い」について勉強していくよ。
そんじゃねー

中学理科の生物では、
という2つの新しい言葉を勉強していくよ。
この2つはぶっちゃけ、
紛らわしい。
前半の2文字が同じで、遠くから見ると同じに見えるからね。
この消化液と消化酵素は一体何が違うんだろう??
ここではその違いをはっきりさせていこう。
一つ一つ丁寧にその意味を確認していこう。
消化液(しょうかえき)とは、
食物を分解する機能を持った液体のこと
だよ。
そして、その消化液の中に
消化酵素(しょうかこうそ)
というものが入っていて、食物を分解する働きを持っているんだ。
この様子を図であらわすとこんな感じ。
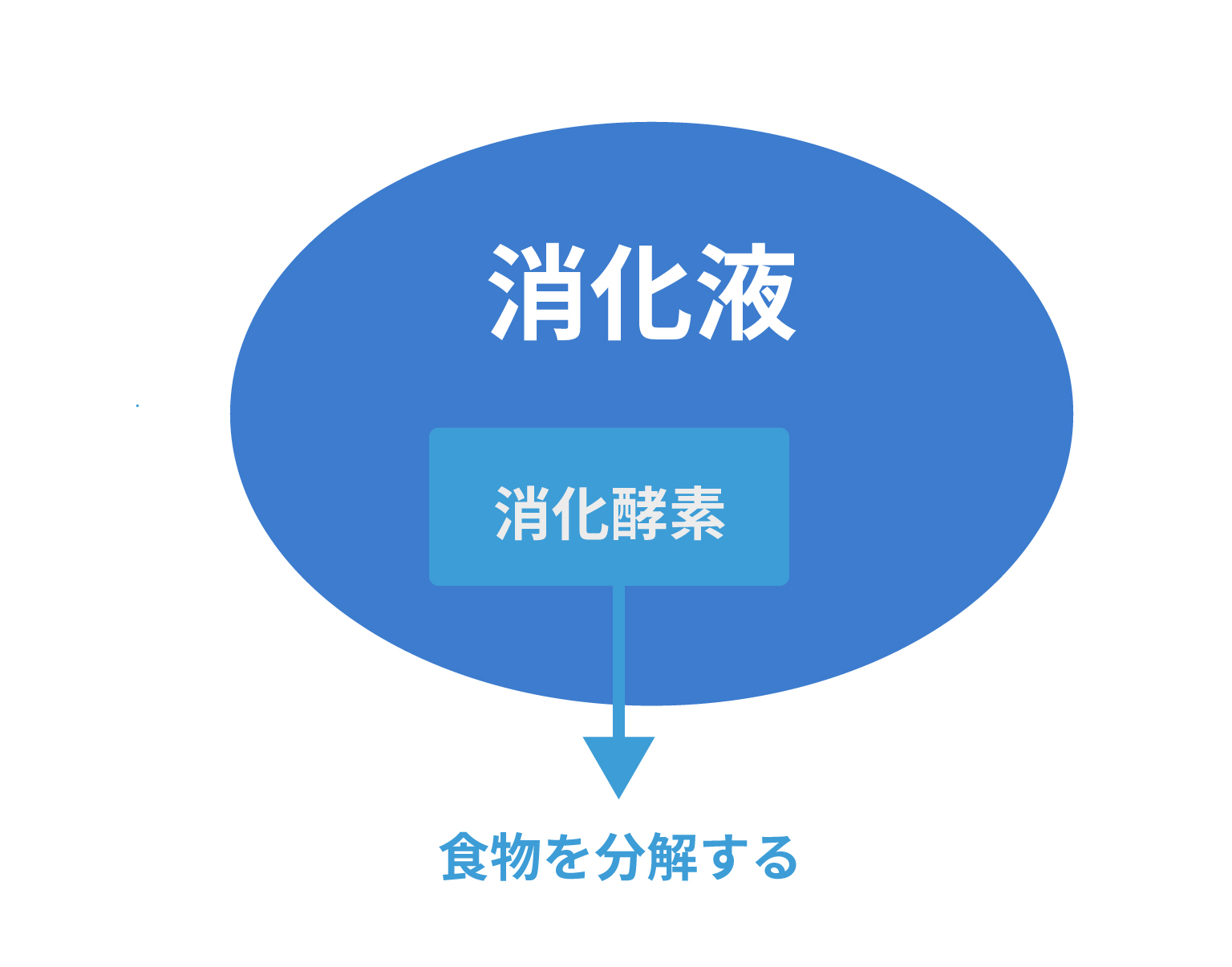
この消化液と消化酵素の関係は車とエンジンの関係に似ているね。

車は高速に移動できる乗り物だよね。
なぜ車は素早く移動できるのか?
それは、車の中にエンジンがあって、そのエンジンで作り出した動力をホイールに伝えられるからなんだ。
この話で言うと、
だよ。

消化液は食物を分解できるけど、なぜ分解できるのかというと、その中の消化酵素が食物を分解する働きを持っているからなんだ。
まとめると、
消化酵素は消化液の1部
ってわけ!
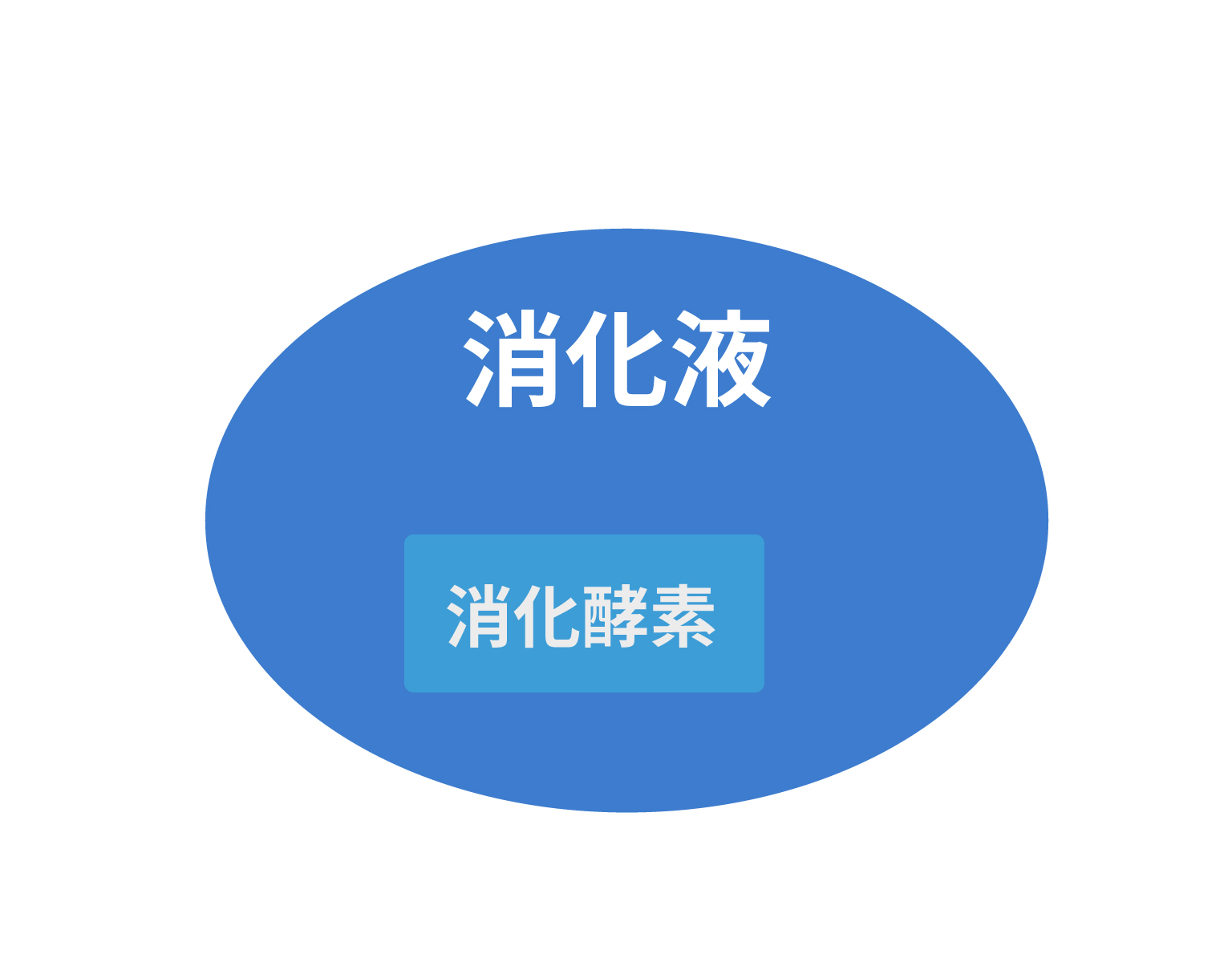
それじゃあ、消化液と消化酵素の具体例を見ていこう。
例えば、つば(だ液)は消化液の1つだよ。
だ液にはアミラーゼという消化酵素が含まれているんだ。
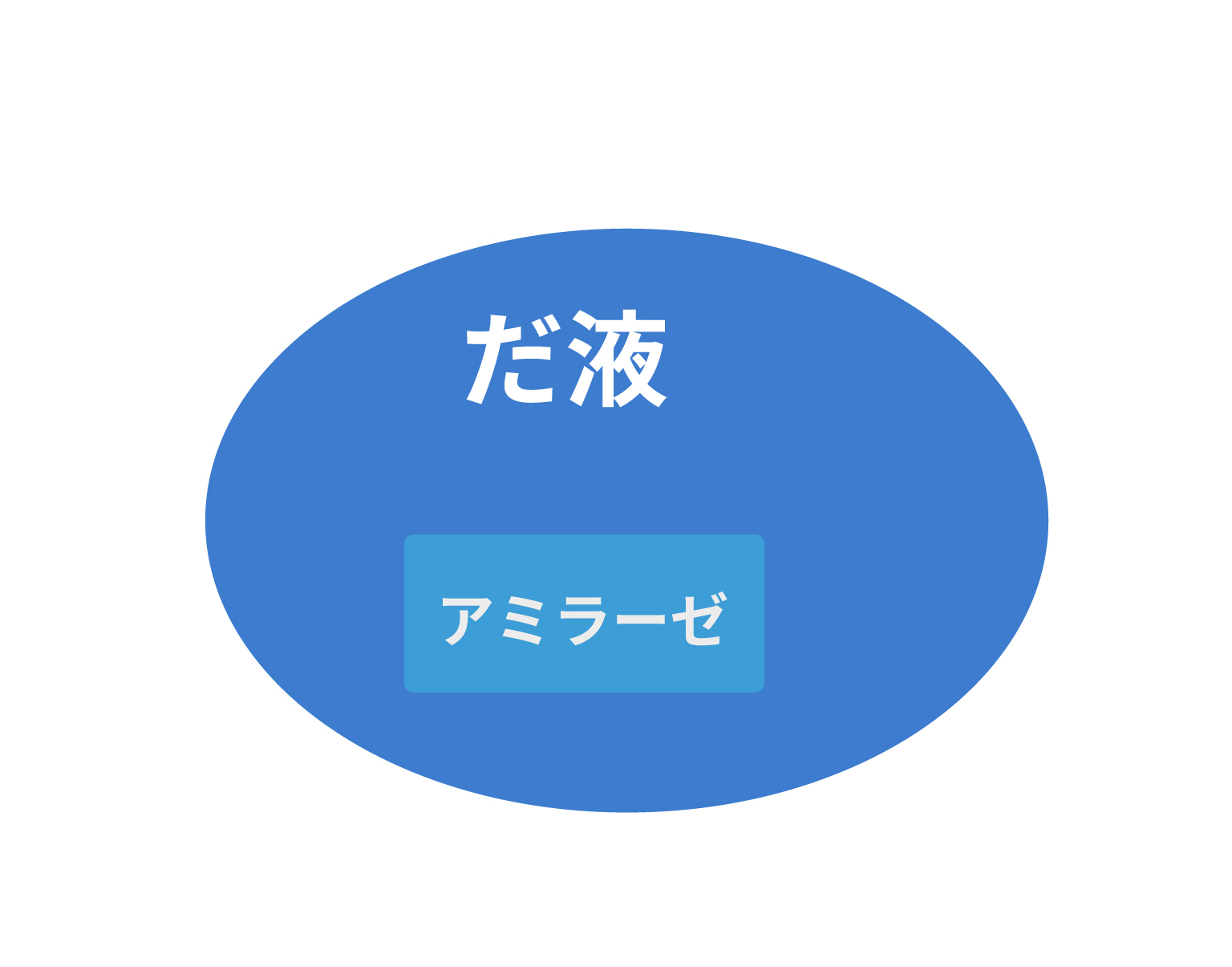
この消化酵素(アミラーゼ)は食物の中にあるデンプンを分解して、麦芽糖に変える働きを持っているのよ。
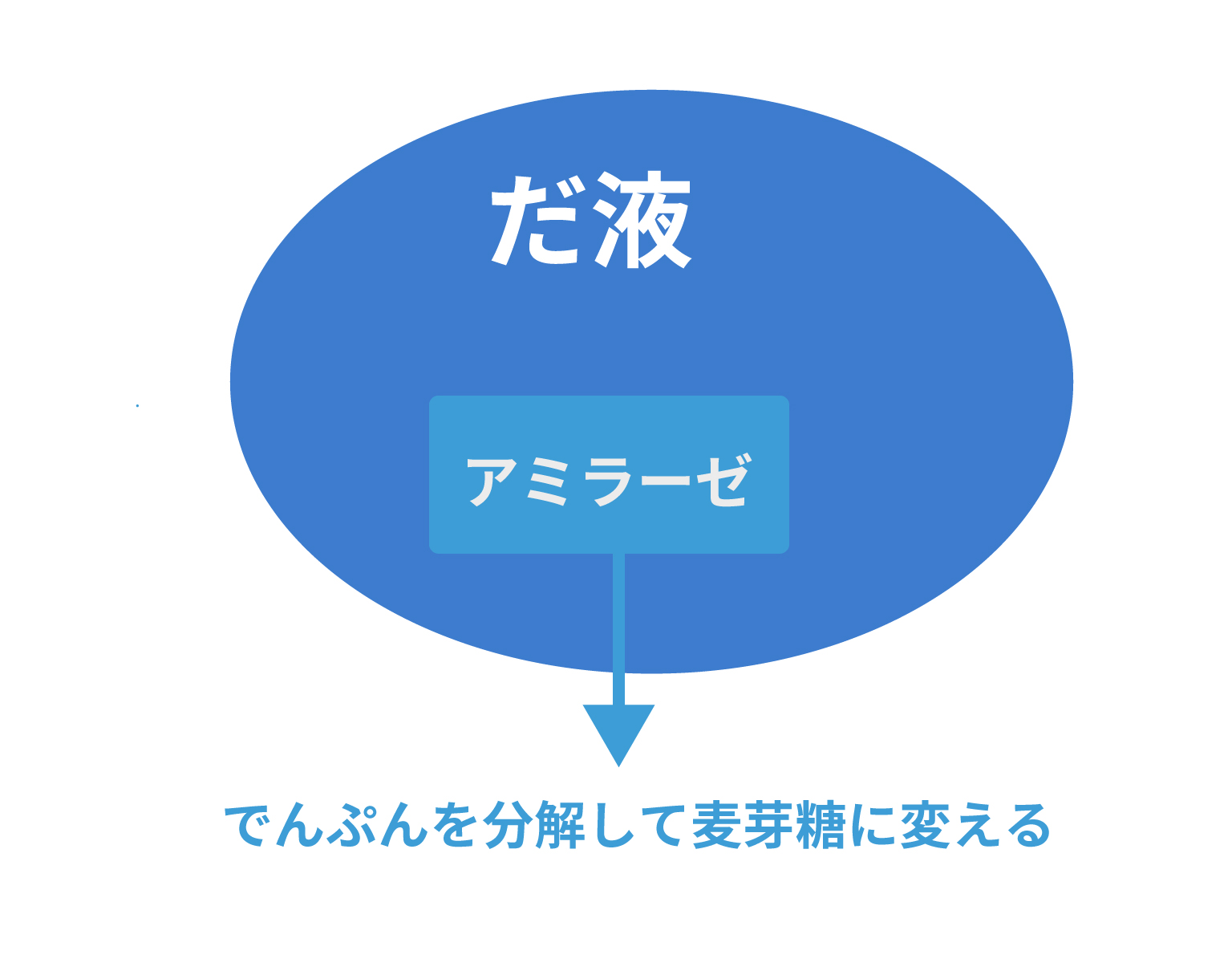
他にも次の表のような消化液と消化酵素のセットがあるのさ。この際チラ見しておこう。

そんじゃねー

生物は、
細胞の数によって2種類にわけられるんだ!
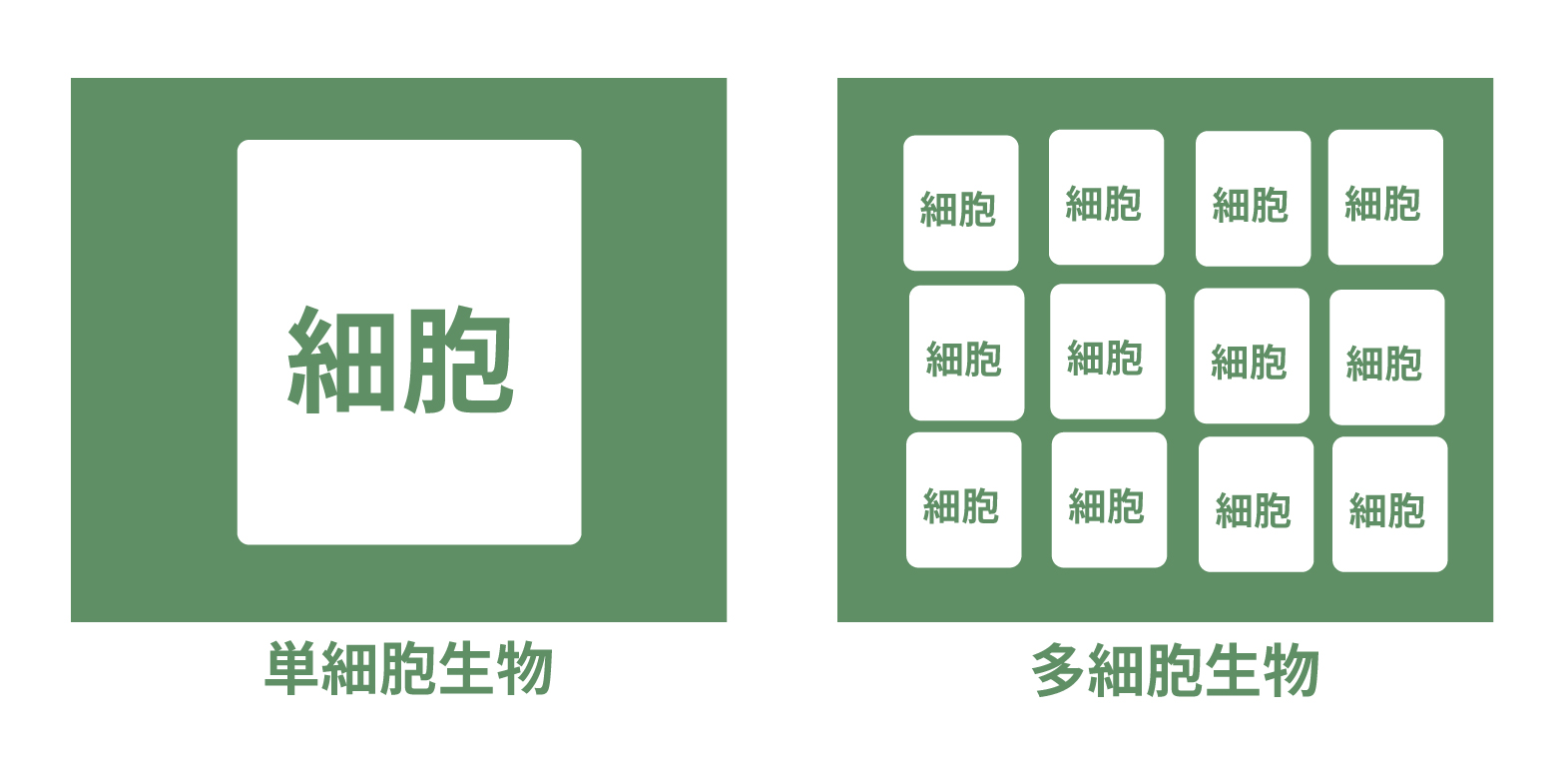
| 単細胞生物 | 1つの細胞で生きる生物 |
|---|---|
| 多細胞生物 | 2つ以上の多くの細胞で生きる生物 |
この2つの生物の違いはもちろん細胞数が違うってことがある。
この細胞数の違いに加えて、それぞれの生物は次の特徴があるよ。
単細胞生物の細胞は1つしかない。

1つの細胞の中に生きるためのすべての機能が備わっているんだ!
例えば、単細胞生物のゾウリムシ。

細胞は1つしかない。
だけど、この細胞の中に多くの機能が備わっているんだ。
まず「べん毛」。
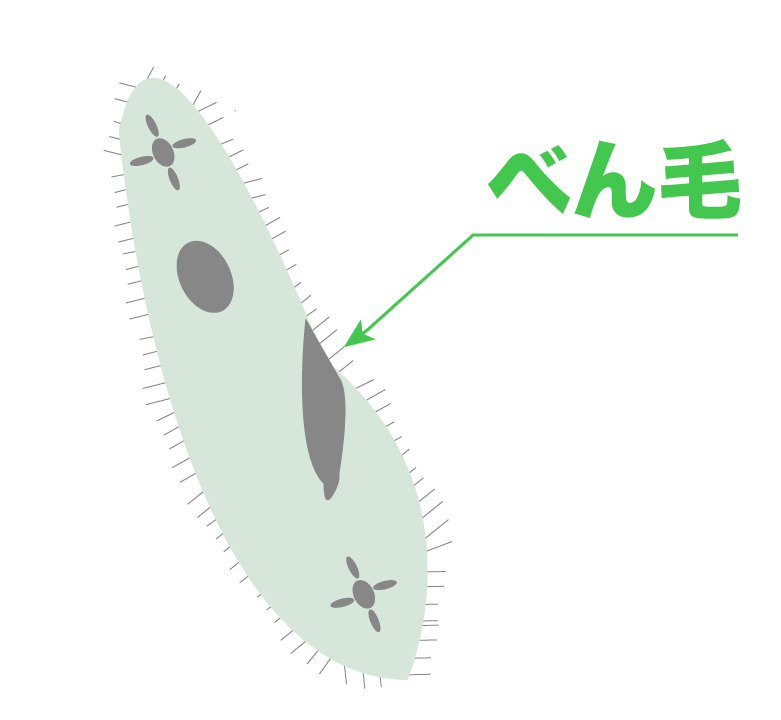
これを動かすことでゾウリムシは自由に泳ぐことができる。
つづいで「口」。
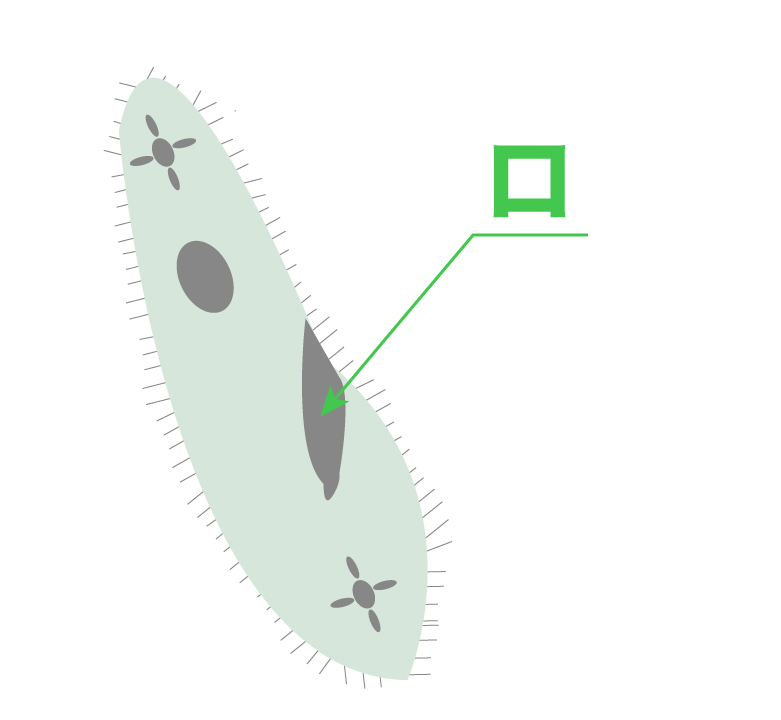
これがあるから、食物を体内に取り込める。
うん、移動できるし外からエネルギーも得られる。
1つしか細胞がなくても生きていけるのが単細胞生物なんだ。
一方、多細胞生物は1つの細胞だけでは生きていけない。
多くの細胞が集まって生きているんだ。

それじゃあ、単細胞生物のほうが強いのか??
いや、そういうわけではない。
多細胞生物では、複数の細胞がグループを作って、生きるための機能を実現しているよ。
が似ている細胞同士がグループを作るのさ。
複数の細胞が集まってできる最初のグループを
組織(そしき)
と人間界では呼んでいるよ。

そして、その「組織」が複数集まって、今度は
器官(きかん)
というさらに大きなグループを作るんだ。
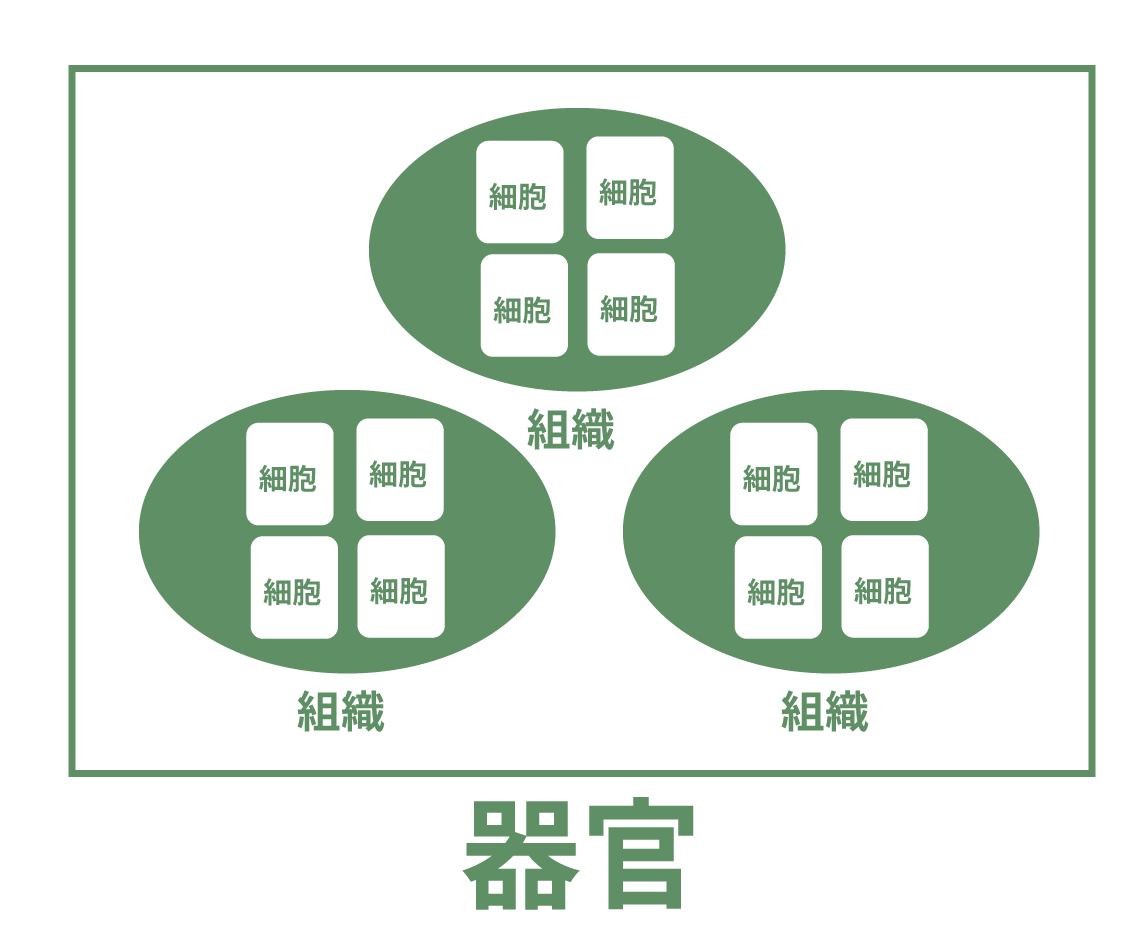
器官は具体的なはたらきを持つ生物のパーツのこと。人間でいうと
とかが器官に当たるね。
そして、その器官が複数集まって今度は
個体(こたい)
を作るんだ。
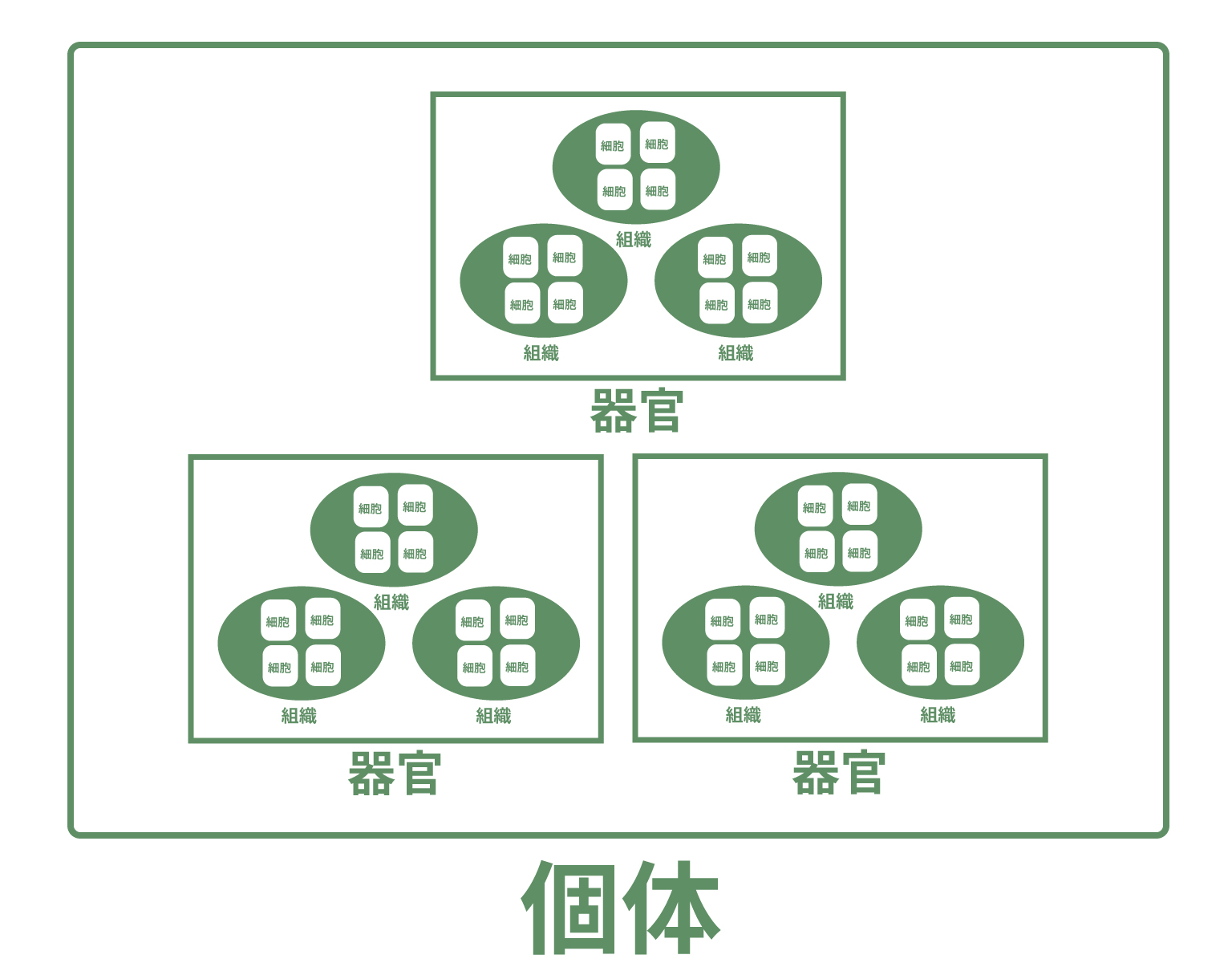
このように多細胞生物では
という3種類のグループがつくられるよ。
小さなグループから徐々に大きなグループを作り、最終的に1つの生物の体(個体)ができあがる仕組みさ。

次は消化液と消化酵素の違いについて勉強していこう。
そんじゃねー

いよいよ中学理科の生物の分野を勉強していくよ。
まず押さえておきたいのが、
細胞(さいぼう)
だね。
細胞とは、
生物を構成する単位の1つさ。
細胞がたくさん集まって生物ができているんだ。
犬や猫もそうだし、もちろん人間だってたくさんの細胞が集まってできているよ。
そして、この細胞というやつは
でその特徴に違いがあるんだ。
ここではこの動物の細胞と植物の細胞の違いを勉強していこう。
まずは動物の細胞から。
動物の細胞は主に次の3つからできているよ。
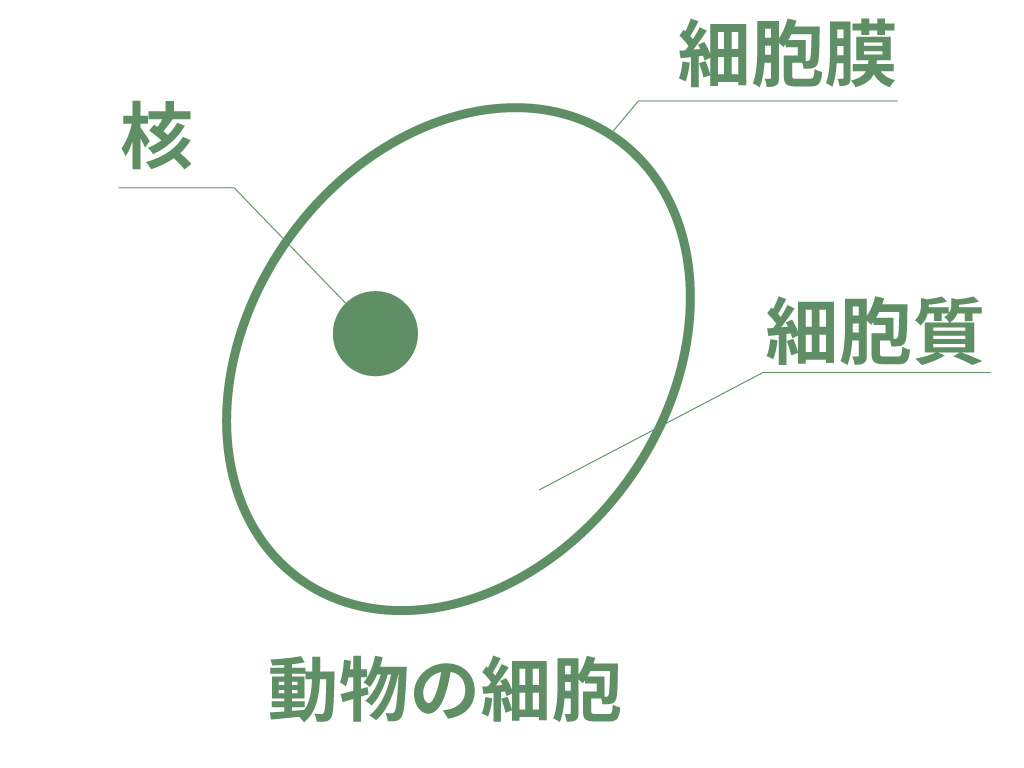
「核」ははどの細胞にも1つあるもの。ここには、その細胞が持つ遺伝情報が含まれているんだ。
つまり、その生物を生み出す元になった生物から受け取った情報が含まれているのね。
そして、細胞の核以外の部分は「細胞質」と人間界では呼んでいるよ。
その細胞質を包んでいるのが「細胞膜」という膜さ。
これが動物の細胞構成する主なものたちだよ。
という3パーツは植物の細胞も持っている。
その他にも次の3つ、植物の細胞はさらに持っているのさ。
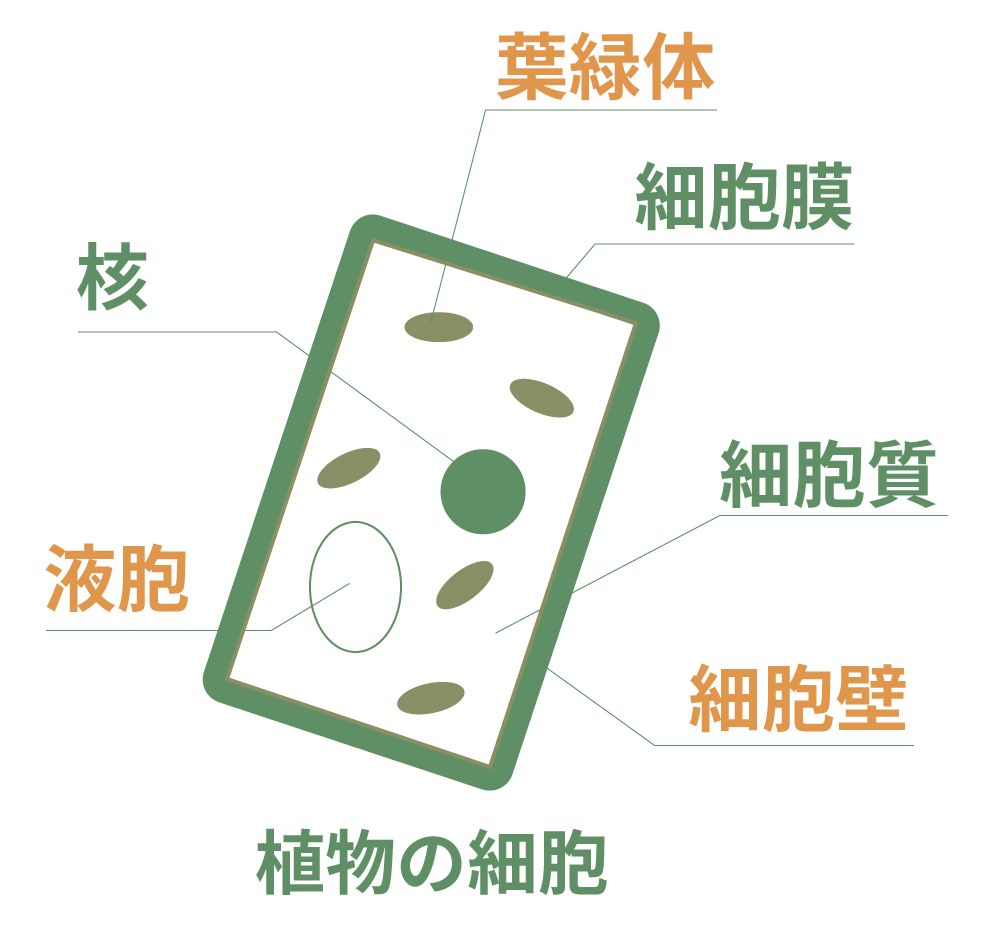
「葉緑体」は光合成を行う場所。
「細胞壁」は、細胞膜の外側を覆っているもの。これがあるから、植物は固くて形を保てるんだ。
最後の「液胞」は、細胞が生きるために活動することで誕生した水やその他の物質が含まれているよ。
このように動物の細胞と植物の細胞は違うことに注意してね。
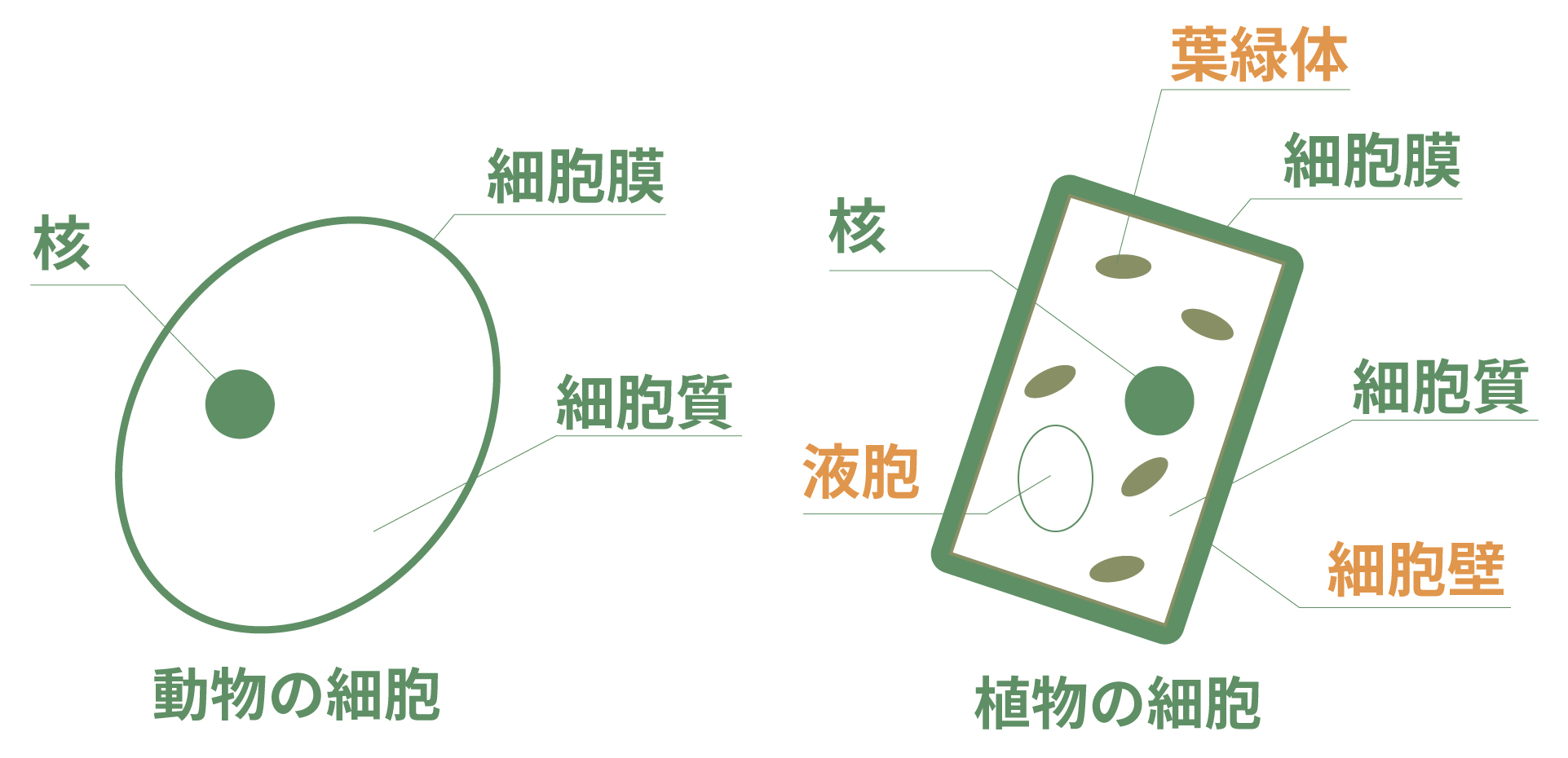
この違いを表にまとめてみたよ。
| パーツ | 役割 | 動物の細胞 | 植物の細胞 |
|---|---|---|---|
| 核 | 遺伝情報をふくむ | ○ | ○ |
| 細胞質 | 核以外の部分 | ○ | ○ |
| 細胞膜 | 細胞質をつつむ | ○ | ○ |
| 葉緑体 | 光合成をおこなう | × | ○ |
| 細胞壁 | 細胞膜をさらにつつむ | × | ○ |
| 液胞 | 細胞の活動で生じたものをふくむ | × | ○ |

そんじゃねー

中学理科の勉強する化学変化の中には
という2種類があるよ。
どちらも「熱」に関係してそうな反応っぽいけど、一体こいつらはどう違うのか??
ここでは、この2つの発熱反応と吸熱反応の違いを勉強していこう。
違いはズバリ、
熱を奪うのか化学変化なのか、
それとも、
熱を発生させるのか化学変化なのか、
だね。
つまり、熱のありなしで違うんだ。
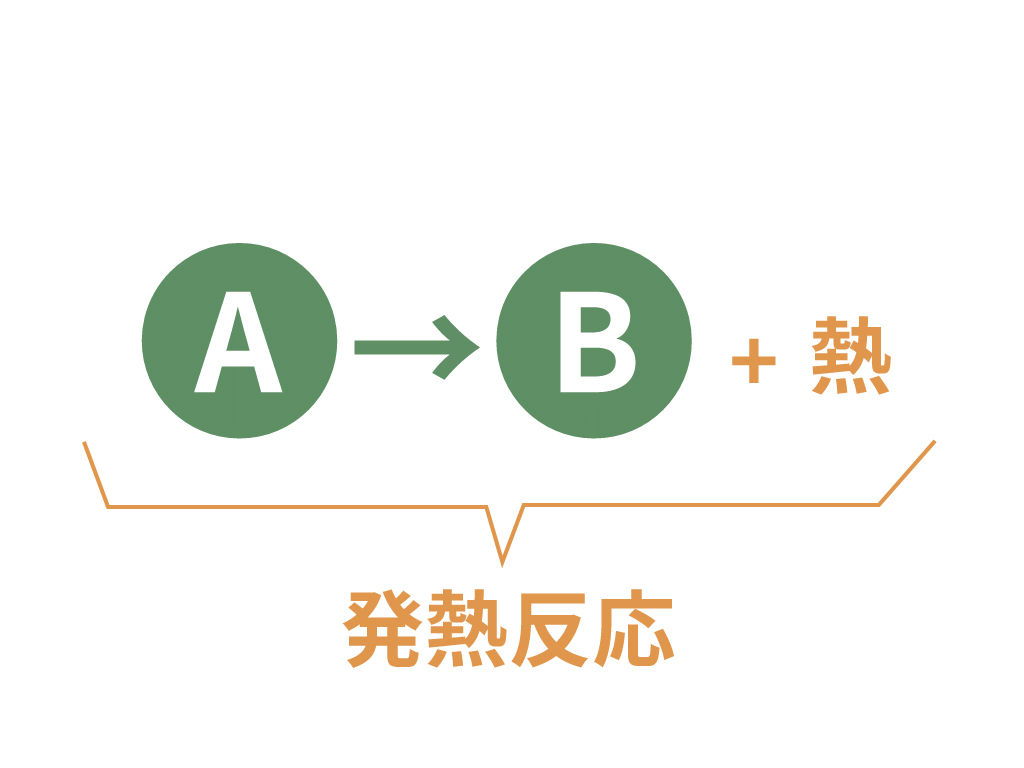
発熱反応は文字通り、
熱の発生というイベントが発生する化学変化のこと
さ。
化学変化とは、
ある物質が別の物質になる変化のこと
だったよね。
ある物質が別の物質になったとき、それと同時に、
周囲に熱を発生させる反応のこと、
これを発熱反応というんだね。
例えば、発熱反応の具体例にはカイロがあるよ。
カイロの中身は鉄粉。

そう、鉄の粉なんだ。
この小さい小さい鉄の塊が、空気中の酸素に触れて酸化する。
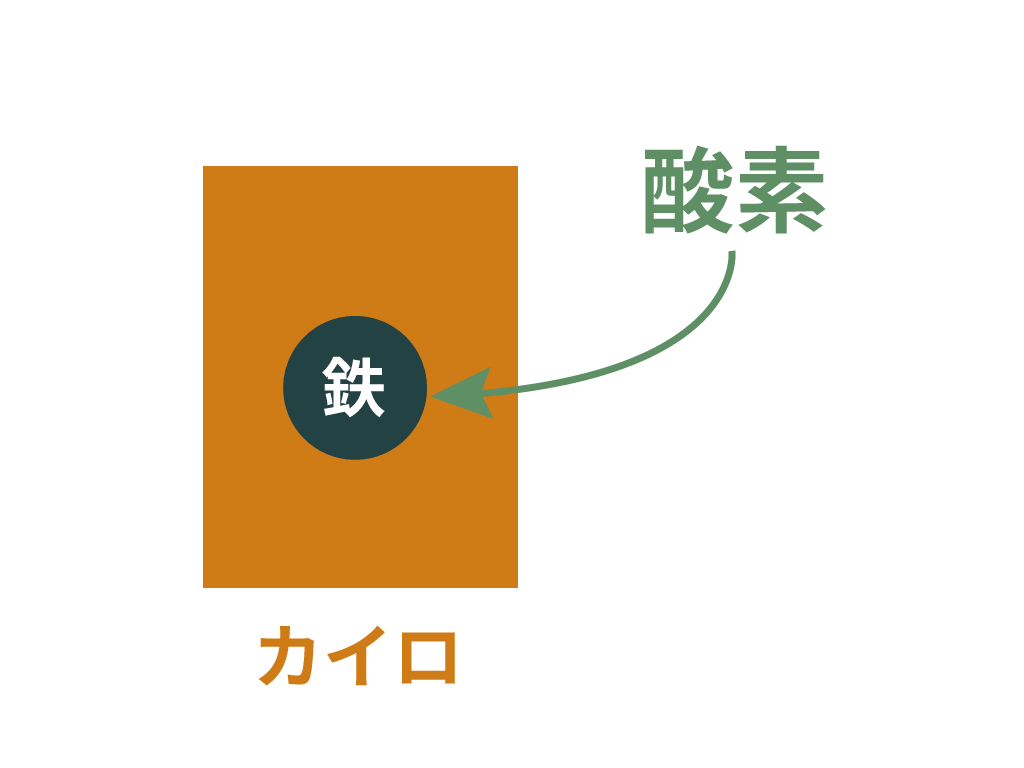
すると、鉄は酸化鉄に進化。
この
$$\ce{鉄 + 酸素 -> 酸化鉄}$$
という反応は発熱反応であることと確かめられているんだ。
周囲に熱をはなちながら反応するのね。
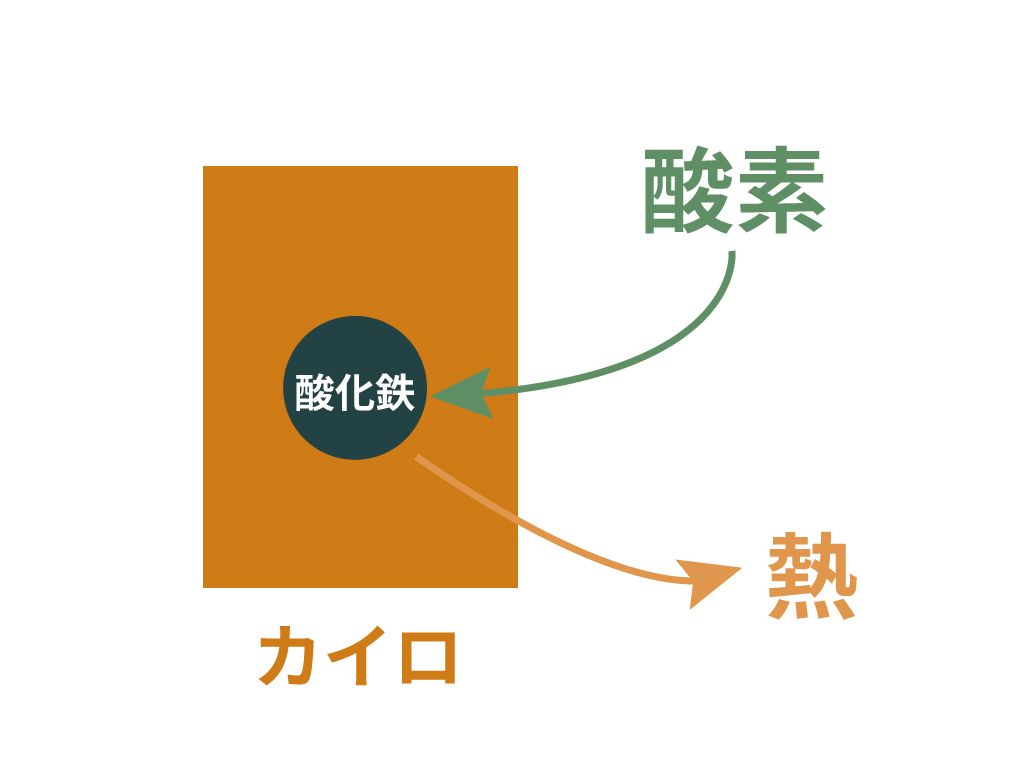
だから、カイロ全体を空気に触れさせてやれば、鉄が酸化されて、酸化鉄になる反応が起きて、ついでに熱も発生させてくれるわけさ。
吸熱反応も文字通り、
周囲から熱を吸い取る、というイベントが発生する化学変化のことさ。
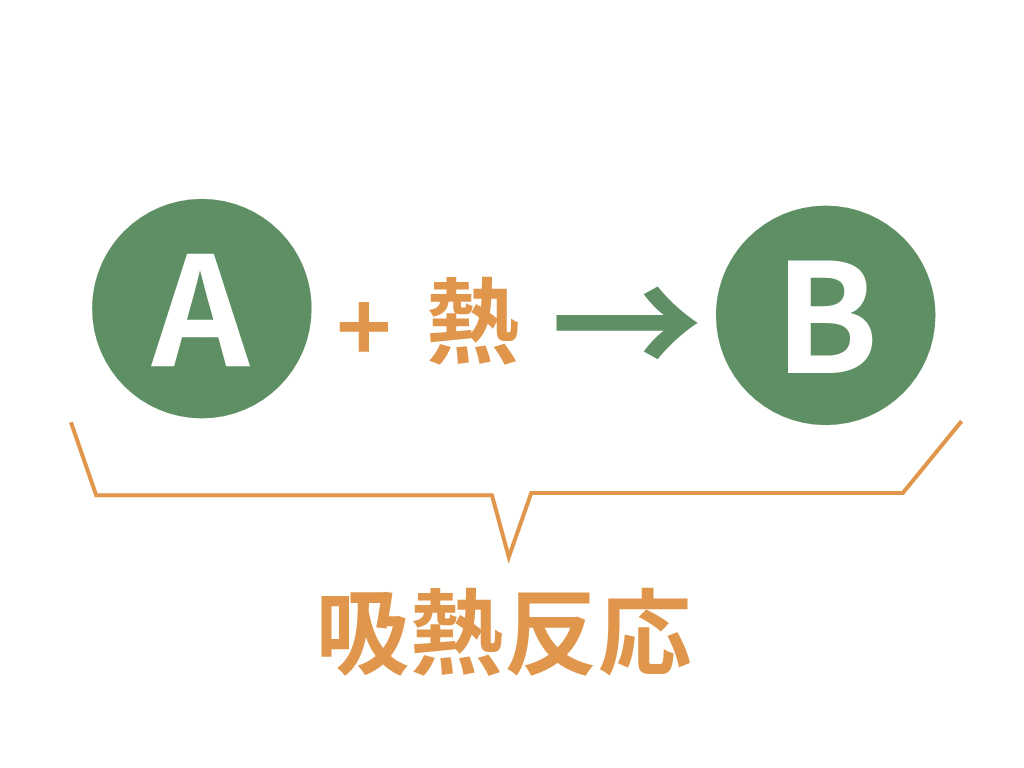
熱の出入りで見ると、さっきの発熱反応とは逆だね。
例えば、冷却パック。
このパックの中身はおもに
が入っている。そして、この2つは別々に分かれているのね。

で、冷やしたくなったお客さんが外から衝撃を加えて水の袋を割る。
そうすると、水と硝酸アンモニウムが混じり合うんだ。

すると、水に硝酸アンモニウムが溶け始めて化学変化が発生。この水と硝酸アンモニウムが一緒になる化学変化は吸熱反応であると実験で確かめらてているんだ。
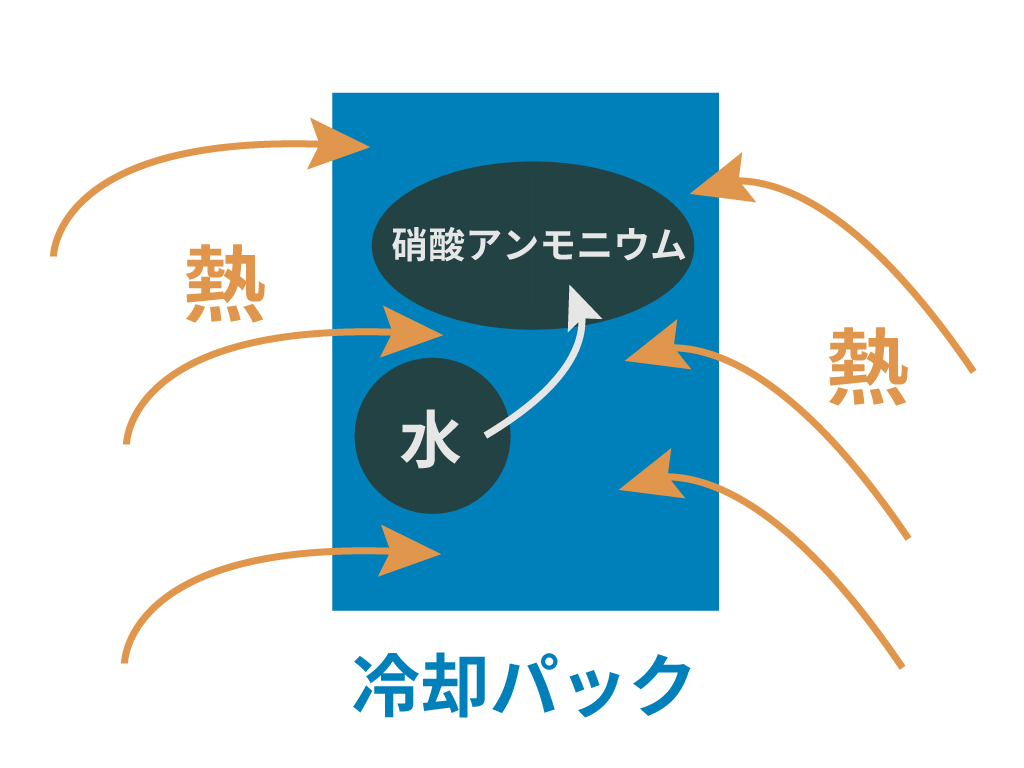
だから、結果的に冷却パックに衝撃を加えてやればパック周辺が冷えるってわけさ。
ここで気になってくるのが、
なぜ化学変化の前後で熱が発生したり熱を奪ったりする現象が起きるのか?
だよね。
じつはこれ、
化学変化の前後で化学エネルギーの差があるからなんだ。
そのエネルギーの差が熱となって出たり、また周囲から熱を奪ったりするのさ。
化学エネルギーとは、
ある物質が持っているエネルギーのこと
だよ。
例えば物質 A にはかけ物質 A の化学エネルギーがあるし、物質 B には物質 Bの化学エネルギーがある。
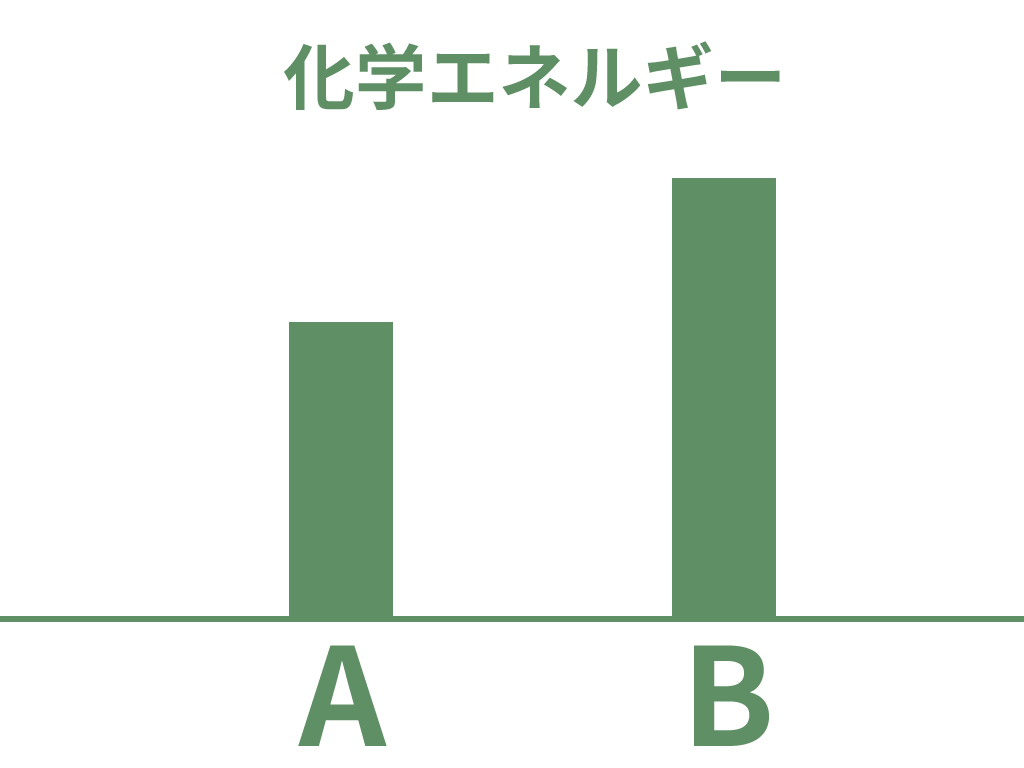
そして、その化学エネルギーの大きさは物質によって異なるんだ。
化学変化の前後でできる物質の化学エネルギーが小さくなったらどうなる?
その時は、そのエネルギー差を埋めるために熱を発生させて埋め合わせるんだ。
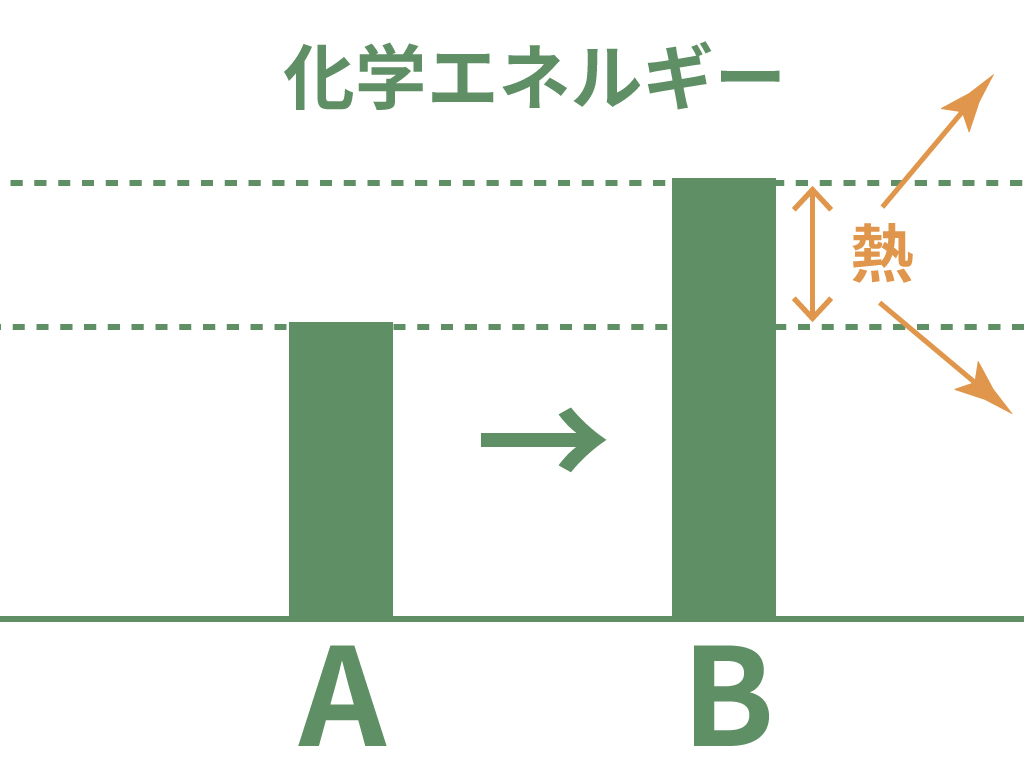
逆に、化学変化して新しい物質になったら化学エネルギーが大きくなったらどうなる?
その時は、周囲から熱を奪うことで化学エネルギーが大きい物質になってその差を埋め合わせるんだ。
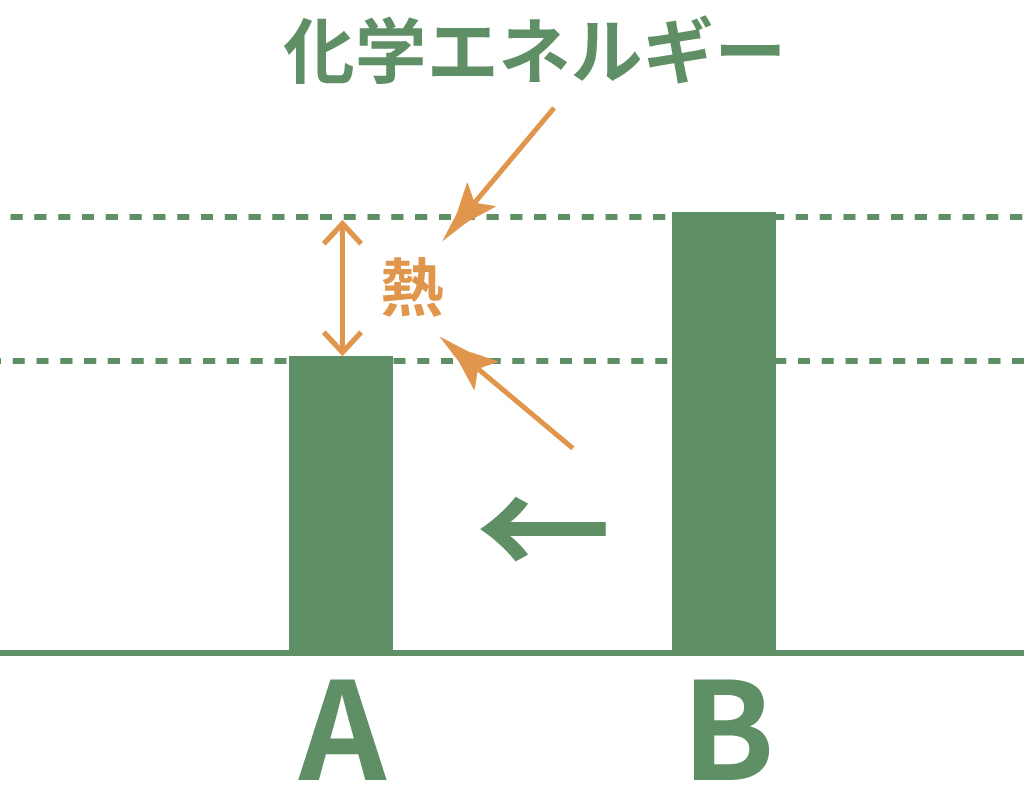
つまりは、
化学変化の前後で化学エネルギーを同じに保とうとする
わけさ。この現象が「発熱反応」と「吸熱反応」になってあらわれているのね。
うん、以上!
ここまでの勉強で中学2年生の理科の化学変化の単元はおしまい。

そんじゃねー

中学理科では、
質量保存の法則
を勉強していくよ。
これは
ある物質が変化して別の物質になってもその質量は変わらない
という法則なんだ。
例えば、物質Aが物質Bと物質Cになったとしよう。
変化する前の物質Aが100 [g] だったとする。
変化後の物質Bと物質Cの質量をたしたら、Aと同じ100 [g] になる!
っていうわけね。
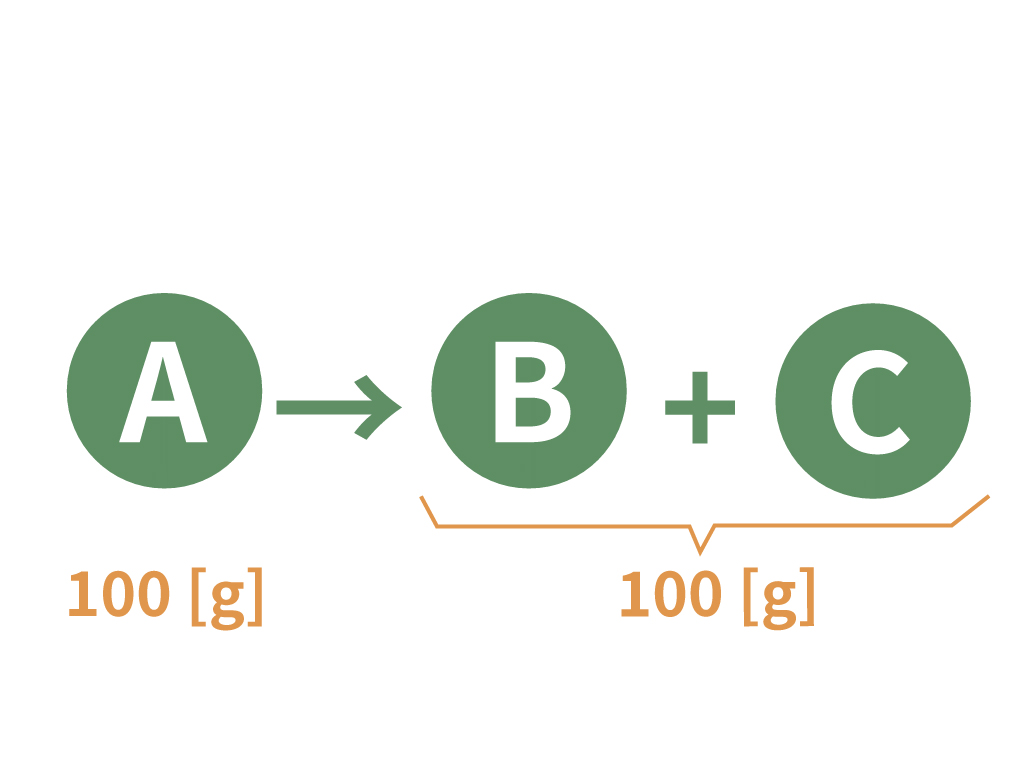
この質量保存の法則は化学変化で有効であるとされているよ。
化学変化とは、
「ある物質」に「あること」をしたら「別の物質」ができること
だったよね。

なぜ、化学変化でも質量保存の法則が使えるのか?
それは、
物質が変化しても、物質を構成している原子は消えない、と考えられるからさ。
さっきの例でいうと、変化前の物質Aの中に入っていた原子たちは、消えてなくなったわけじゃない。
物質Bと物質Cに分かれて散らばっただけと考えるのさ。
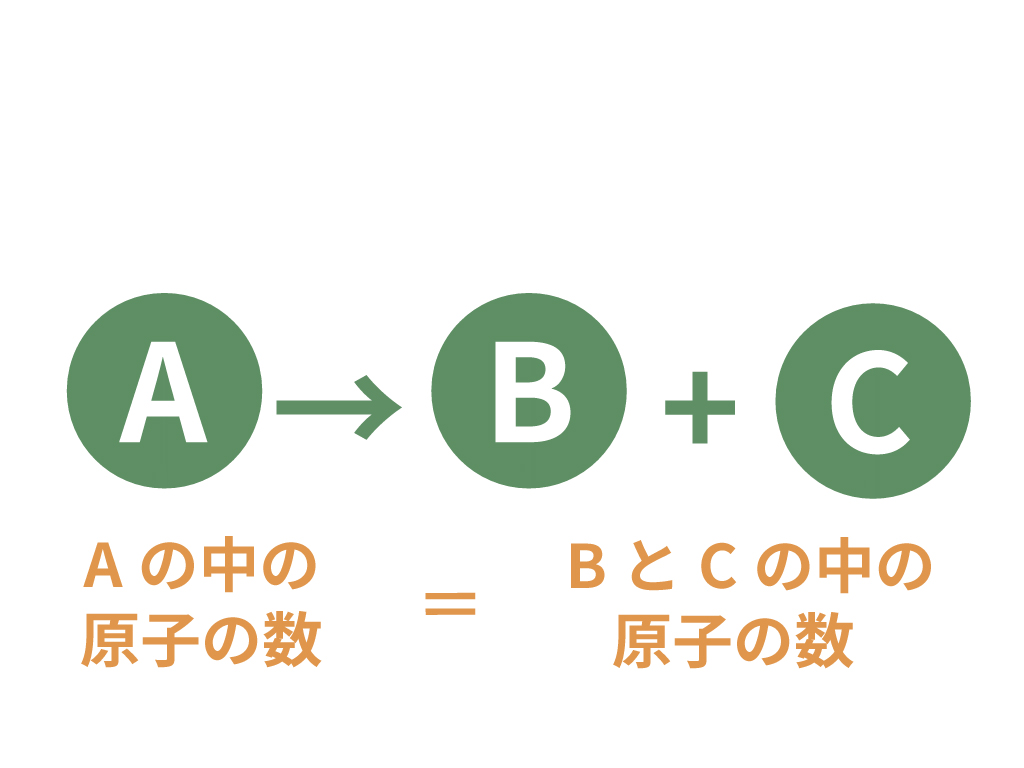
それぞれの原子の重さが同じとするなら、変化前の物質Aと、変化後の物質Bと物質Cの質量の合計は変わらないんだね。
そんな質量保存の法則の具体例を見てみよう。
例えば、水素と酸素が合体して水になる化学変化。
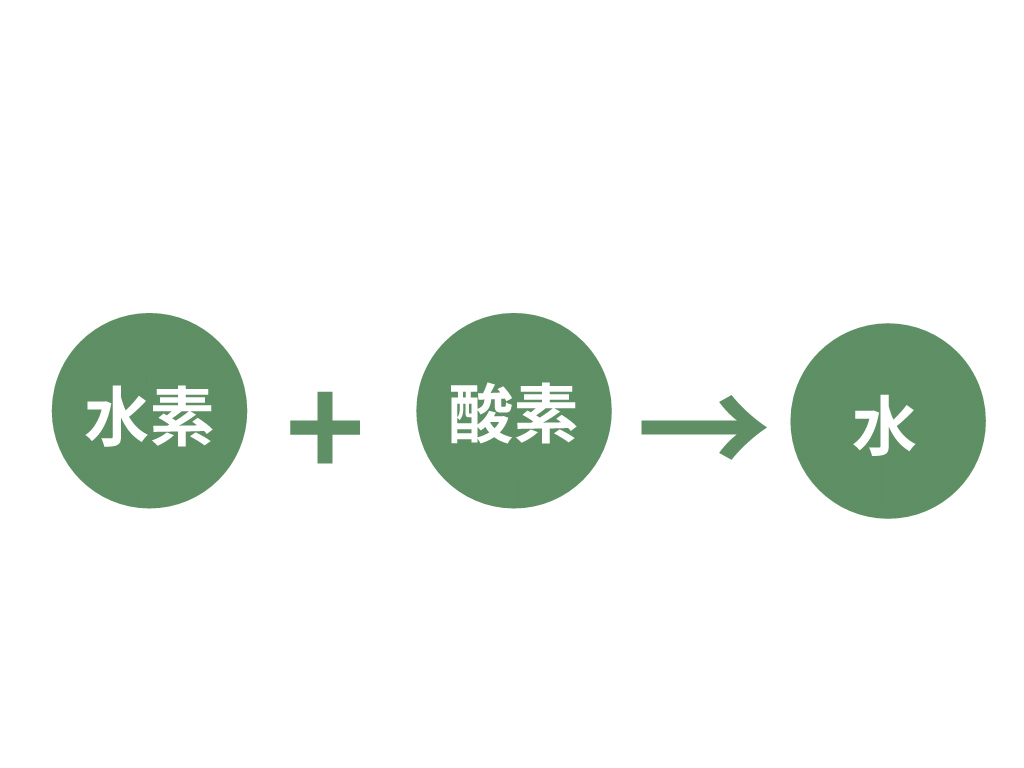
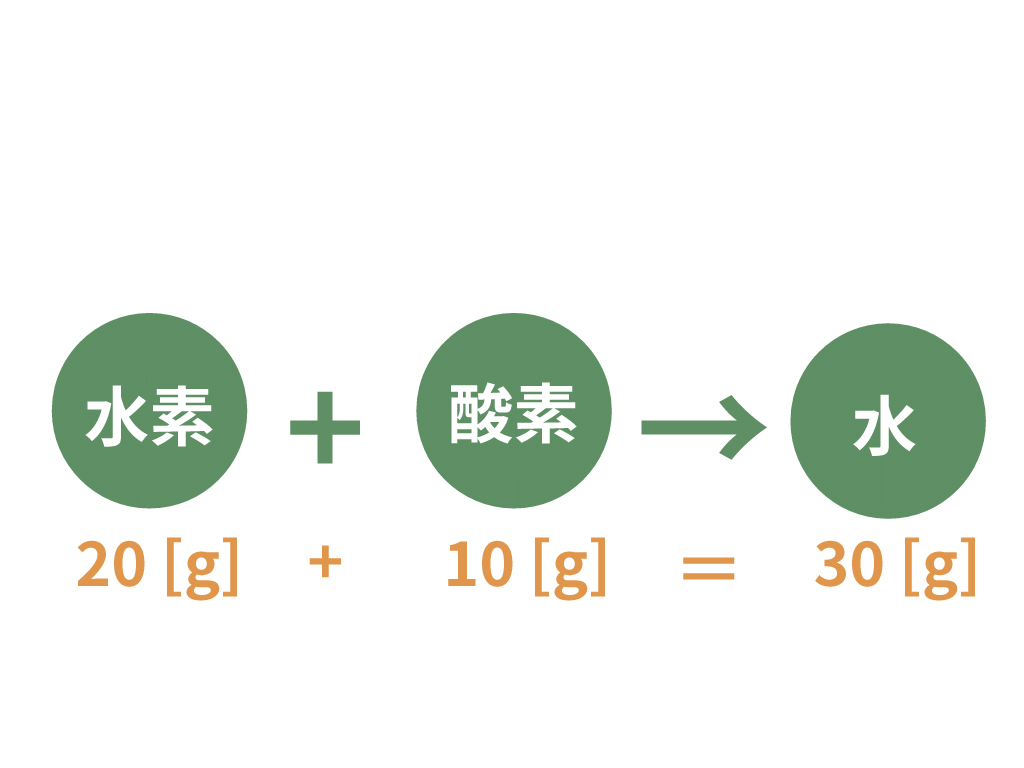
水素が20 [g]、酸素が10 [g] だったら、新しくできる水はどれくらいの重さになるかな?
そう、そいつらを合わした質量の30 [g] ってことになるんだ。
この質量保存の法則は化学変化だけじゃなくて、物理変化でも有効と確かめられているよ。
物理変化とは、
物質の形が変わるだけで、物質の中身はそのままの変化のこと
だね。
また、中1理科で習った「状態変化」でもこの質量保存の法則は有効とされるよ。
うん、以上。

そんじゃねー

前回、酸化を勉強してきたね。
酸化とは、
ある物質が酸素と結びついて新しい物質ができること
だったことを思い出そう。
今回は、その逆の反応の、
還元(かんげん)
を勉強していくよ。
「酸化の逆」ってことはつまり、
何かが酸化物と結びついて、酸化物から酸素を取りのぞく反応さ。
これを人間界では「還元」と呼んでいるんだ。
例えば、酸化物 A に、ある物質 B が結びついたとしよう。
結果、物質 C と D ができたんだ。
物質 C は、酸化物 A から酸素をとっぱらって新しくできた物質さ。
物質 D 物質 B と 酸素が化合してできた酸化物だ。
この反応で「酸化物 A」 が 「酸化物じゃない物質 C」 になることを「還元」というんだ。
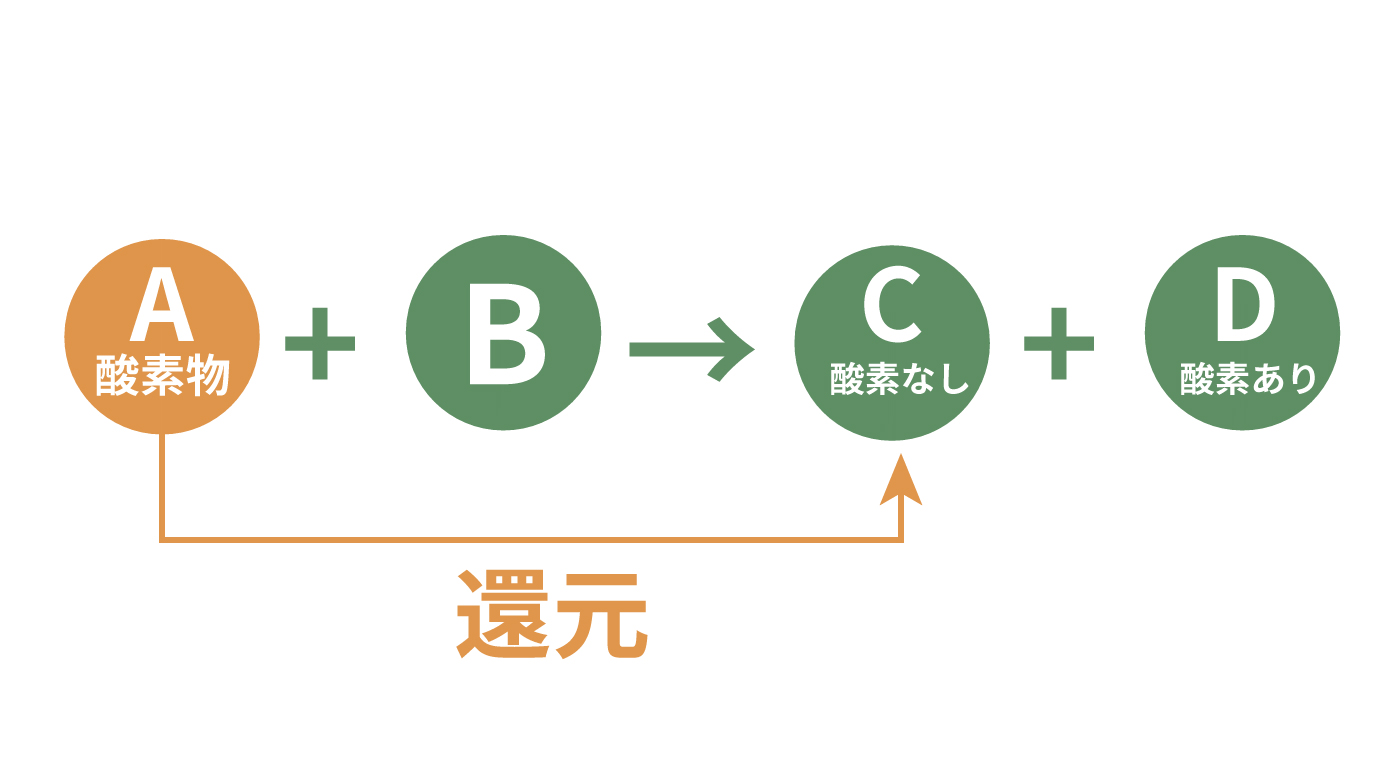
ここで注目したいのは、
還元と酸化は同時に起こる!
ということね。
さっきの例を振り返るよ。
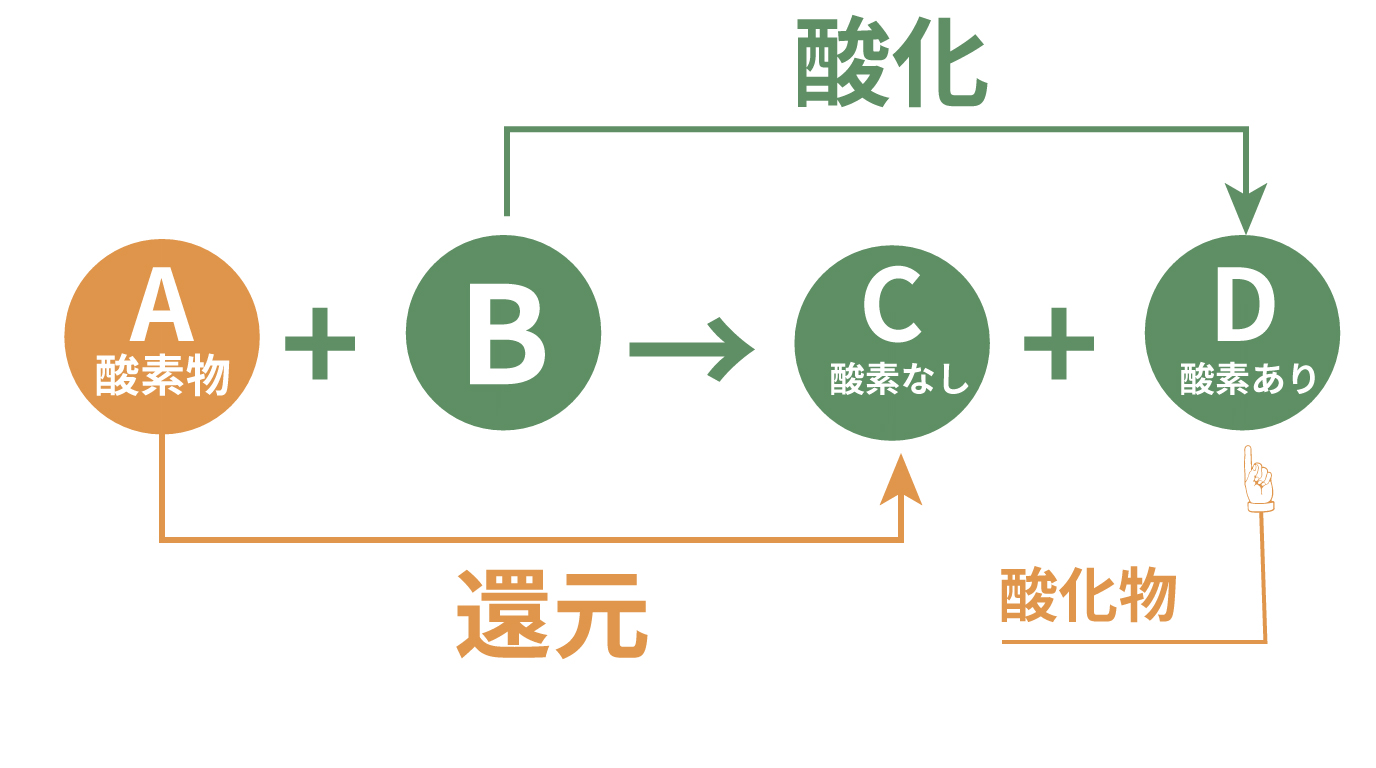
還元を引き起こした超本人の物質 B が酸素と結びついて物質 D になった。
酸素と結びつく反応は新しい物質ができる反応は「酸化」と言ったよね。
だから、この「物質 B が物質 D になる反応」は「酸化」だ。
新しくできた物質 D は
酸化によってできた化合物
だから「酸化物」ということになる。
このように、今回勉強した「還元」は「酸化」とセットで同時に起こることも頭に入れておこう!
最後に還元の具体例を見ていこう。
例として、
が結びついていく反応を想像して。
この化学反応式は次のようになるね。
$$\ce{CuO + H2 -> Cu + H2O}$$
酸化銅$\ce{CuO}$の酸素$\ce{O}$が取っ払われて、同時に水$\ce{H2O}$ができる反応さ。
酸化物の酸化銅$\ce{CuO}$から酸素$\ce{O}$が取り払われるこの反応を還元、水素と酸素が結びついて水$\ce{H2O}$になる反応を酸化、新しくできた水を酸化物だね。
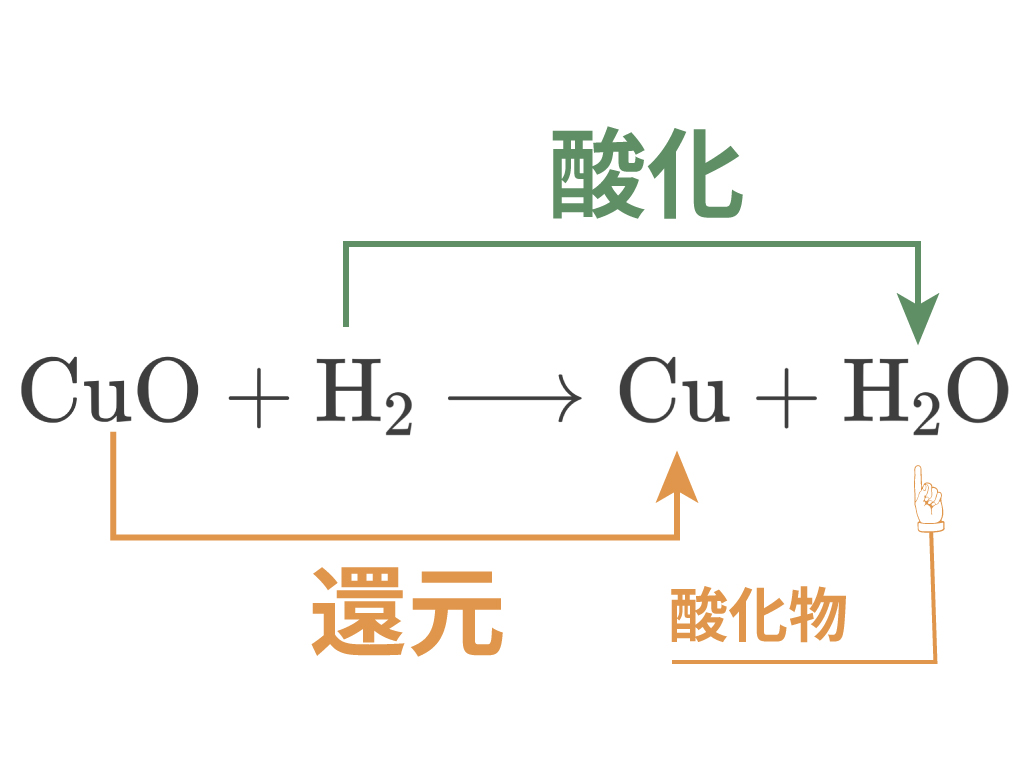

ということまでおさえれば還元はオッケー。次は質量保存の法則を勉強していこう。
じゃあねー

中学理科では、
という2つのキーワードが登場するよ。
こいつら一体どう違うんだろうね??
今日はこの酸化と燃焼の違いをはっきりさせておこう。
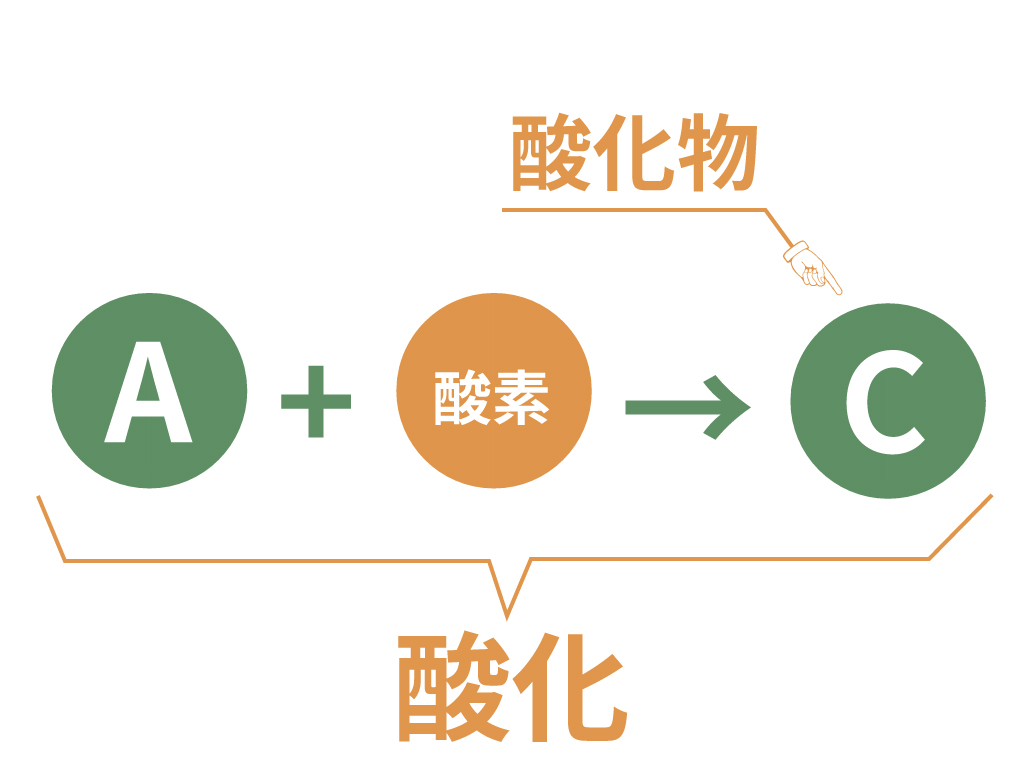
酸化とは、
ある物質が酸素と化合すること
をいうよ。
「化合」を復習すると、
2種類以上の物質から新しい物質ができること
だったよね。
例えば、物質Aと物質Bが結びついて、新しい物質Cができること。これが化合さ。
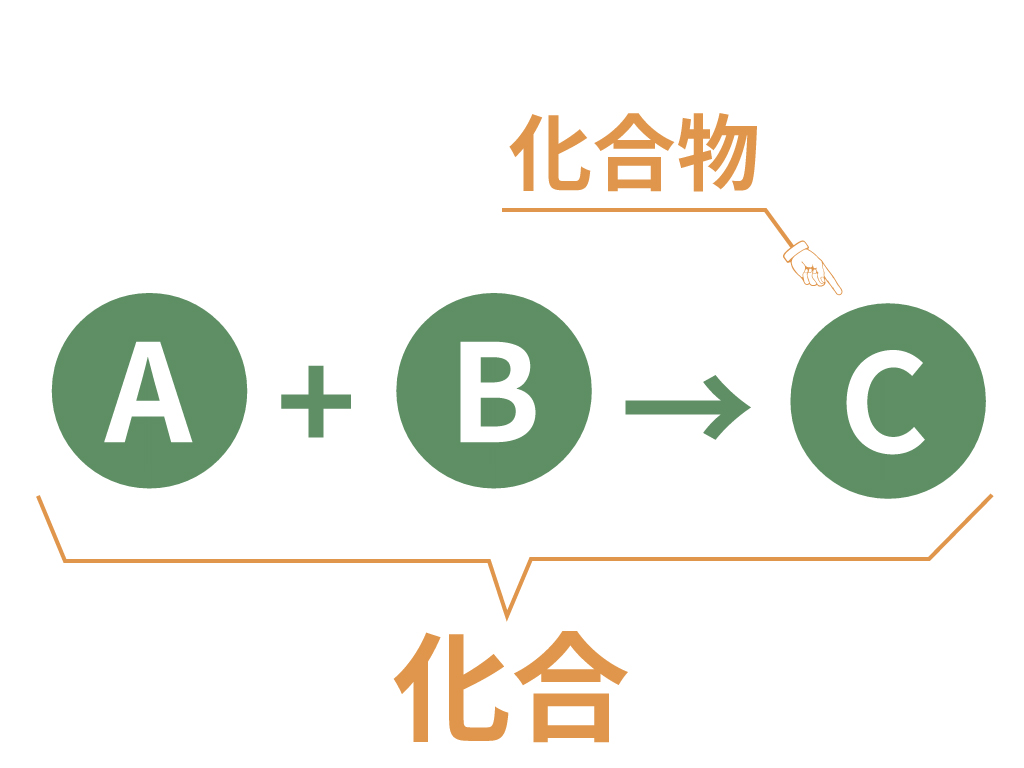
そして、新しくできた物質Cを「化合物」と呼んでいたことを思い出そう。
そして、ここで勉強する「酸化」はなんと、
化合の1種!
反応前の物質A、Bのどちらかが「酸素」であるとき、その化合は「酸化」と呼ばれているんだ。

そして、新しくできた物質Cは「酸化物」というのさ。
例えば、
が結びついて酸化銅ができる反応は酸化の一種だね。
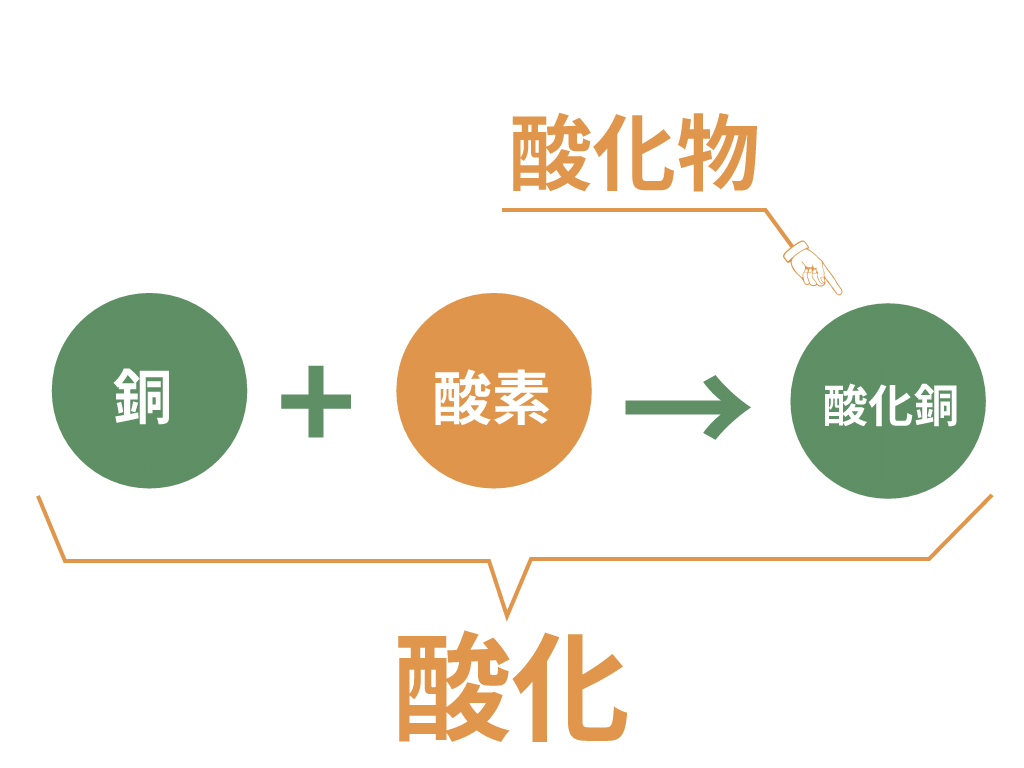
化学反応式で書くと次のようになる。
$$\ce{2Cu + O2 -> 2CuO}$$
続いて、燃焼だね。
燃焼とは、
ある物質が熱や光を出しながら酸化されること
をいうんだ。
さっきの例でいうと物質Cという酸化物に加えて、
も一緒に出る酸化を「燃焼」というんだ。
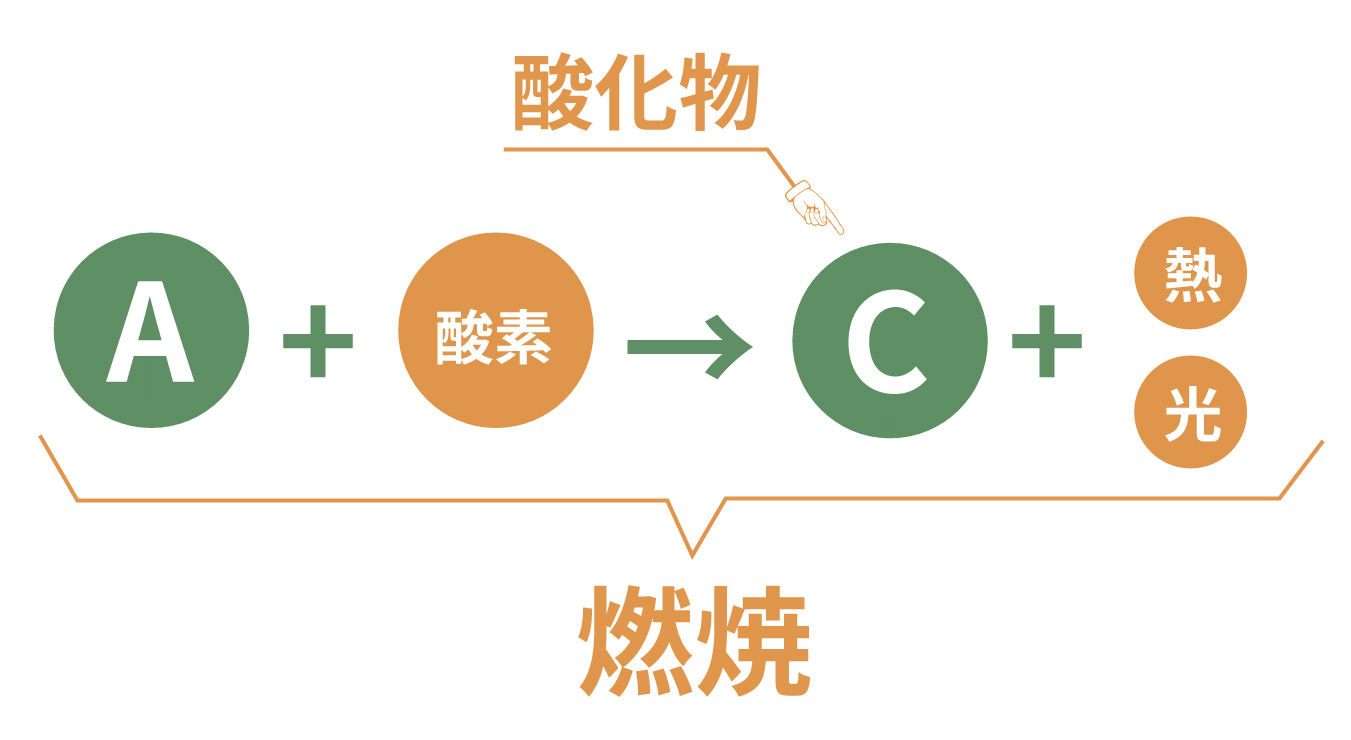
その燃焼の1つの例としてよく出てくるのが、
が反応して酸化マグネシウムができる反応さ。
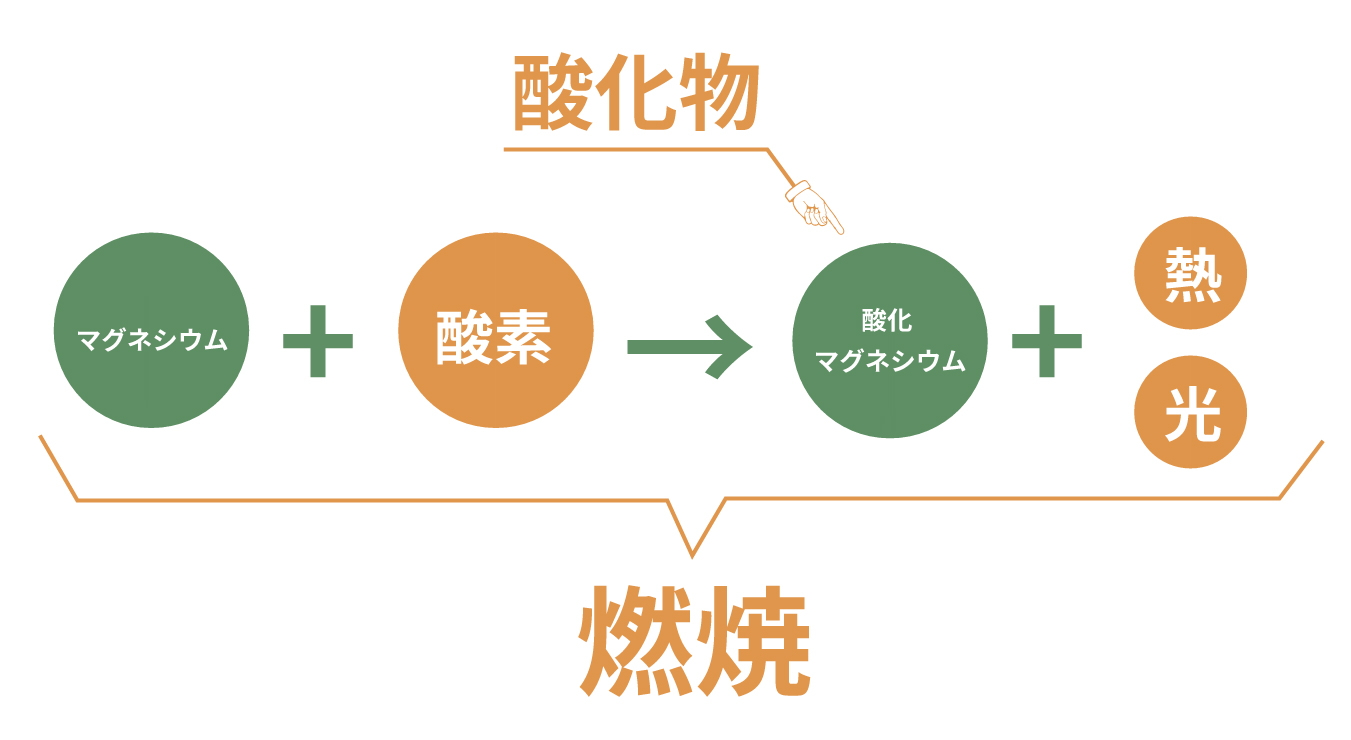
化学反応式は次のものだね。
$$\ce{2Mg + O2 -> 2MgO}$$
マグネシウムは空気中の酸素と化合すると熱や光を出すんだ。
ってことで、燃焼と酸化の違いはズバリ、
燃焼は酸化の1種類である
ということだ。
世界の酸化にはいろんな酸化があるんだけど、燃焼はそのうちの1つ。
このことを図で表す次のようになるよ。
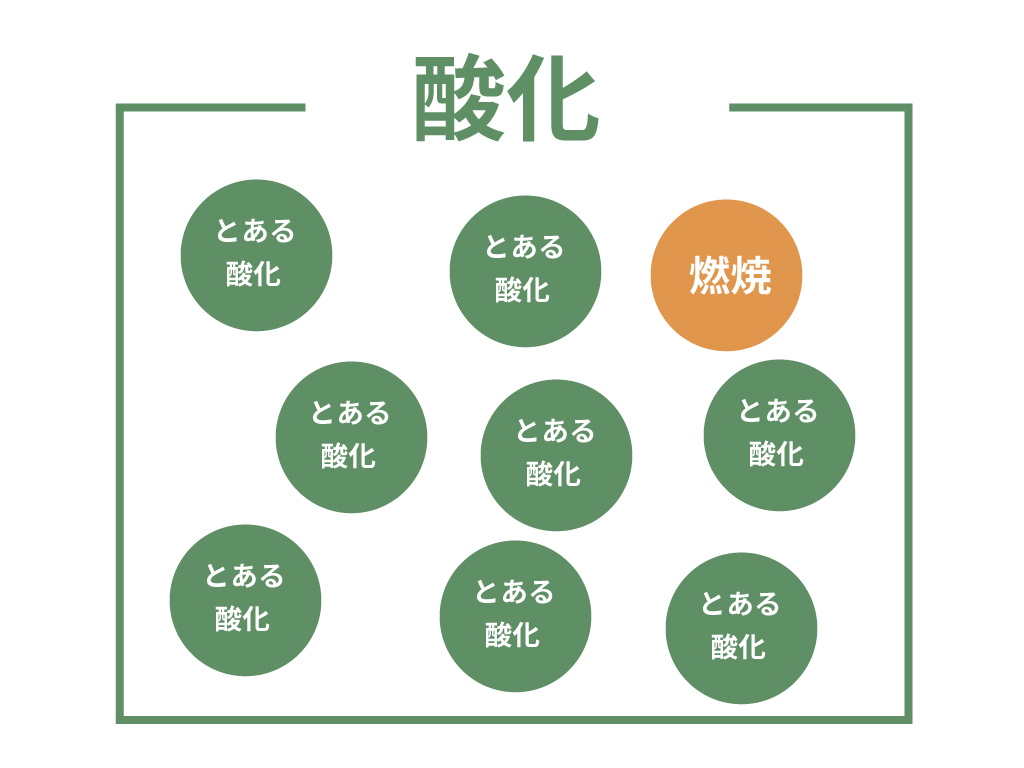
この関係は・・・そうだな、文房具と鉛筆の関係さ。
文房具っていろんな種類の文房具があるよね。
鉛筆とか、消しゴムとか、シャーペンとか、もういろいろ。
そんでもって、鉛筆はその文房具の1種類であるに過ぎないんだ。
つまり、
鉛筆は文房具である
と言えるけれども、
文房具は鉛筆である
とは言えない関係なんだ。
文房具は酸化、燃焼は鉛筆と考えるとわかりやすいよ。
つまり、
燃焼は酸化である
けれども、
酸化は燃焼ではない
んだ。

そんじゃねー

ここでは、
化合(かごう)
を勉強していこう。
化合とは、
2種類以上の物質から新しい物質ができる化学変化のこと
だよ。例えば
が化学変化を起こして、新しい物質Cになったとしよう。
このような化学変化を化合、新しくできた物質を化合物と人間界では呼んでいるんだ。

化合の身近な例として、
水素と酸素から水ができる化学変化があるよ。
水素と酸素を混ぜて火をつけると、音が鳴って水ができる、っていう実験やったよね。
「水素」と「酸素」という2種類の物質が化学変化を起こして新しい「水」という物質になった現象なんだ。
このような現象を「化合」、新しくできた水が「化合物」さ。
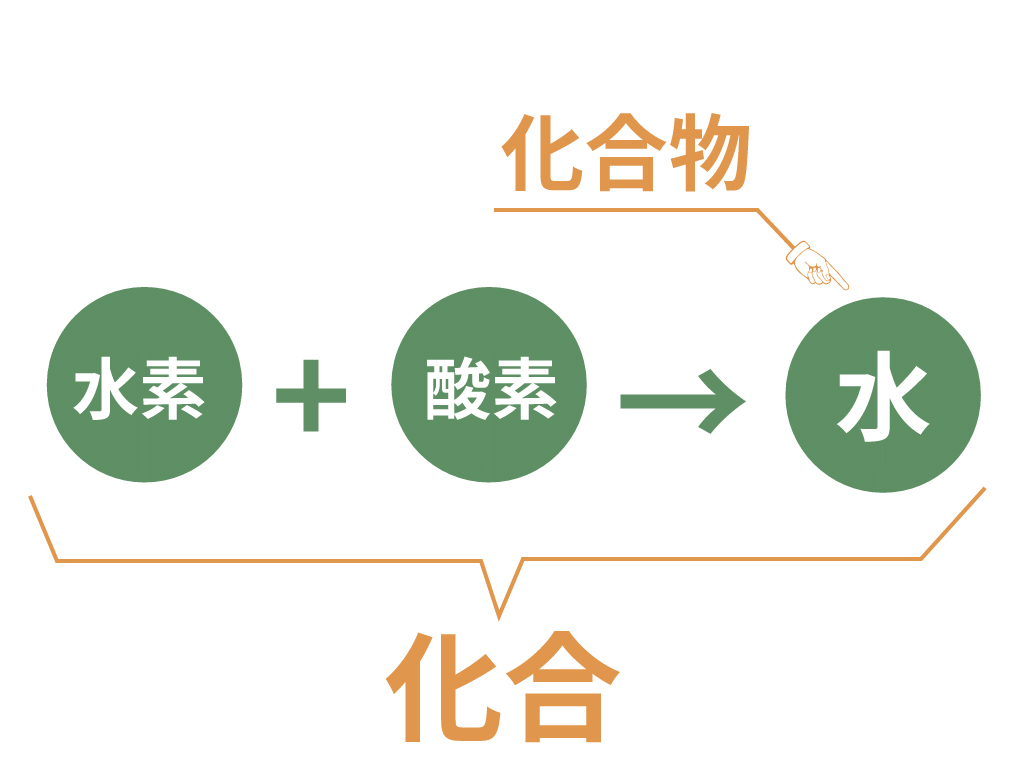
それじゃあ、ここまでで勉強してきた化学変化との違いは何なんだろうね。
ずばり、
化合は化学変化の1種に過ぎないんだ!
この様子を図で表すとこんな感じ。
つまり、化学変化には化合意外の種類も存在しているってわけ。
その化合以外の化学変化の1つの例として、
分解があるね。
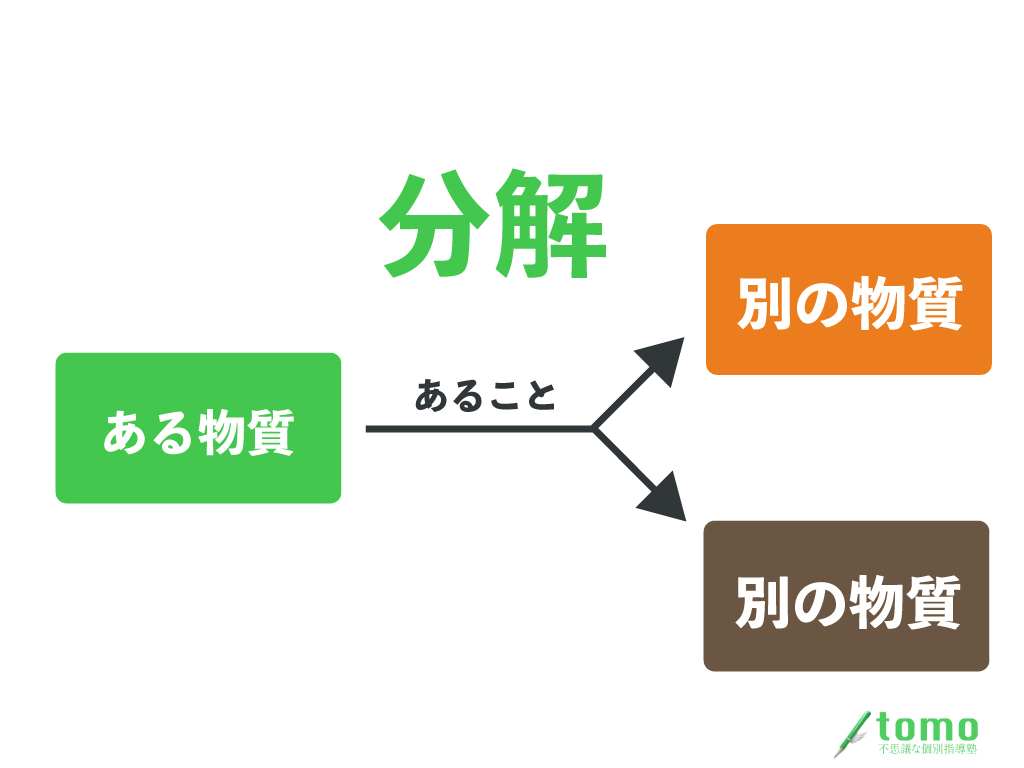
分解とは、
「ある1種類の物質」に「あること」をしたら「2種類以上の物質になること」
だったよね?
野菜に例えるなら、化学変化が野菜。
で、そのうちの野菜のうちの1つのトマトが化合に当たるってわけだ。
野菜には他にも、キャベツ、ナス、ピーマン・・・・があるよね。
それと同じで、たくさんある化学変化の1種類が化合であるんだ。だから、化合は化学変化であるけど、化学変化は化合ではないんだ。
トマトは野菜だけど、野菜はトマトでないのと一緒だね。
それじゃあ分解と化合の違いはなんだろうね。
分解はちょうど化合とは反対の化学変化だって考えるとわかりやすいね。
分解とは、
「ある1種類の物質」に「あること」をしたら「2種類以上の物質になること」
だったね。
一方、化合は
2種類以上の物質から新しい物質ができる化学変化のこと
だった。
分解と化合はともに化学変化の1つであることは間違いない。
けれども、その意味は逆で化学変化の内容は異なる、ってことを頭に入れていこう。

そんじゃねー

ここでは、
の違いを勉強していこう。4つも用語が出てきて大変だけど、1つ1つクリアしようね。
まずは「混合物」と「純粋な物質」の違いから。
すべての物質は
にわけられるのさ。
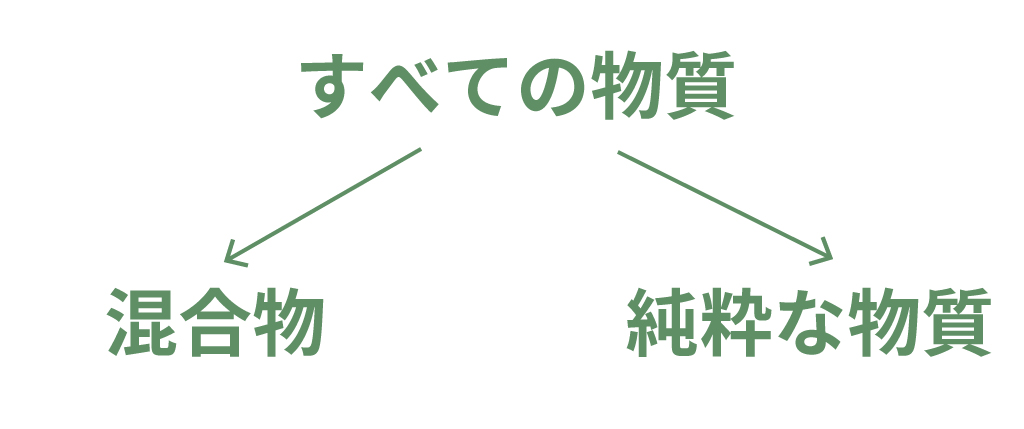
純粋な物質とは、
1種類の物質で成り立っている物質
だよ。

例えば、水とか、水素とか、酸素だね。
こいつらはどう解剖しまくっても、1種類の物質しか出てこないんだ。水ならどこまで行っても水、ってわけ。
混合物とは、
2種類以上の純粋な物質から成り立つ物質だよ。
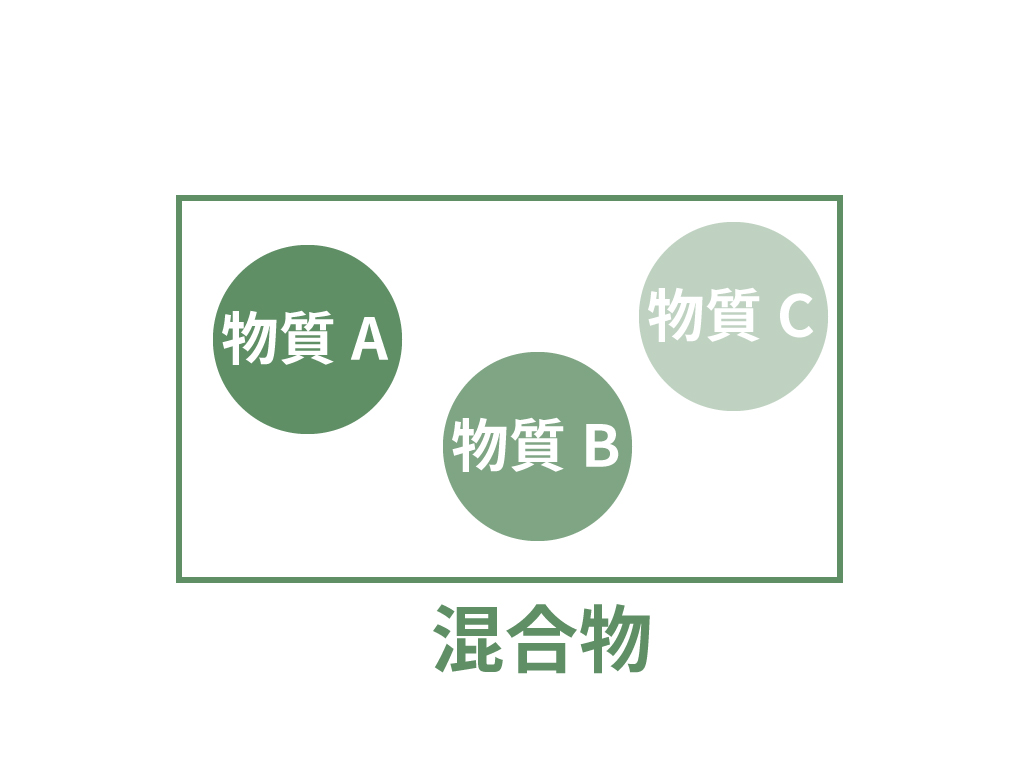
例えば、空気は混合物さ。
「空気」という物質は存在していないんだ。空気の正体は、
といった複数の純粋な物質の気体が組み合わさってできているんだよね。
この「空気」のような物質を人間界では「混合物」と呼んでいるよ。
純粋な物質と混合物の違いもしっくりきたかな?
今度は「単体」と「化合物」の違いを見ていこう。
混合物は一旦脇に置いておいて「純粋な物質」を詳しく掘り下げるんだ。
実はこの純粋な物質、さらにさらに、
に細かく分類できるのさ。
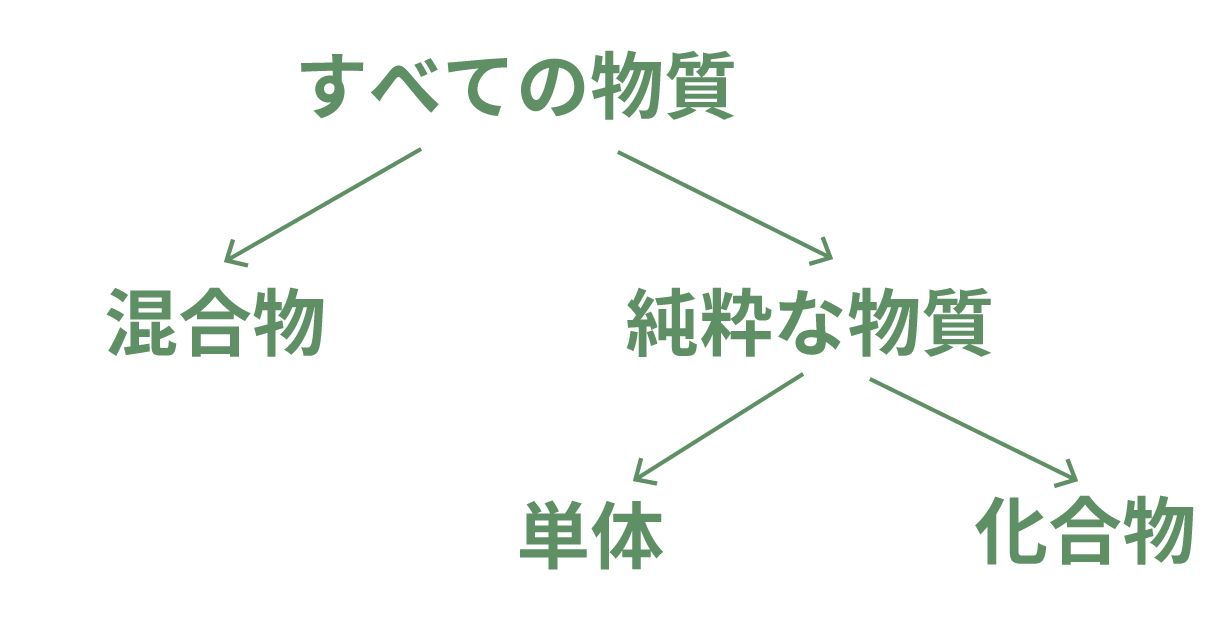
単体とは、
1種類の原子から成り立つ純粋な物質だよ。
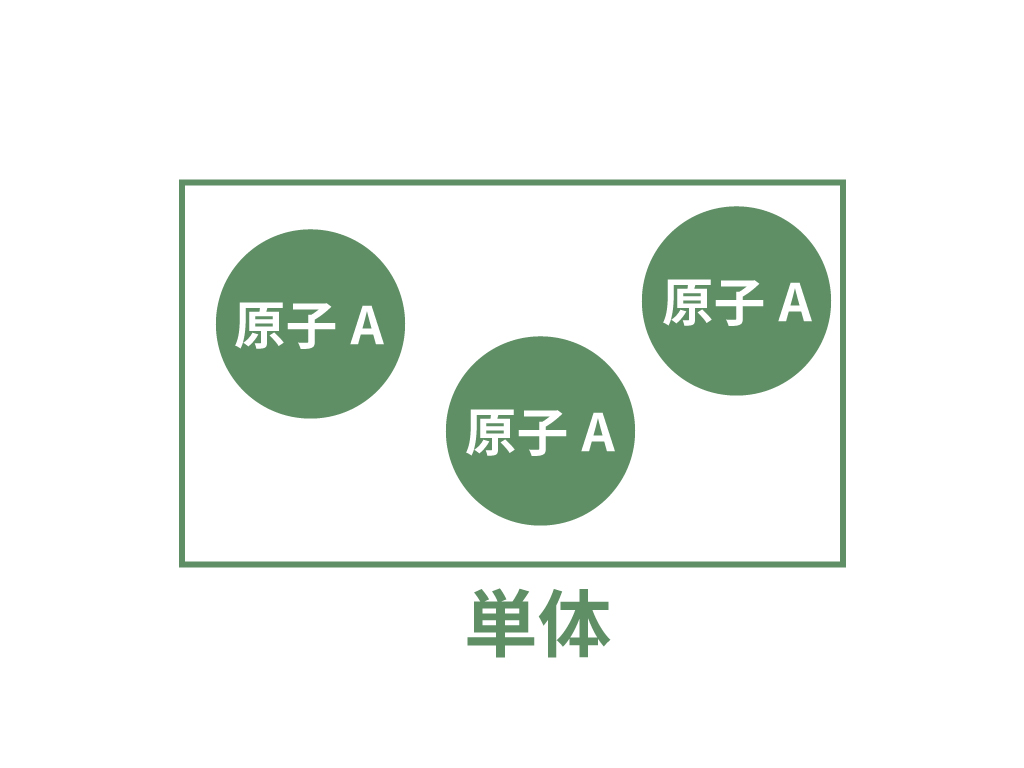
例えば、酸素や水素。
こいつらは単体に該当するね。
分子をつくって複数の原子が集まってもノープロブレム。
ポイントは、1種類の原子でできているか、ってことなんだ。
複数の原子が集まってできていても、全部の原子が同じで1種類なら、それは単体に分類されるのさ。
そいで、化合物とは、
2種類以上の原子から成り立つ純粋な物質
だよ。
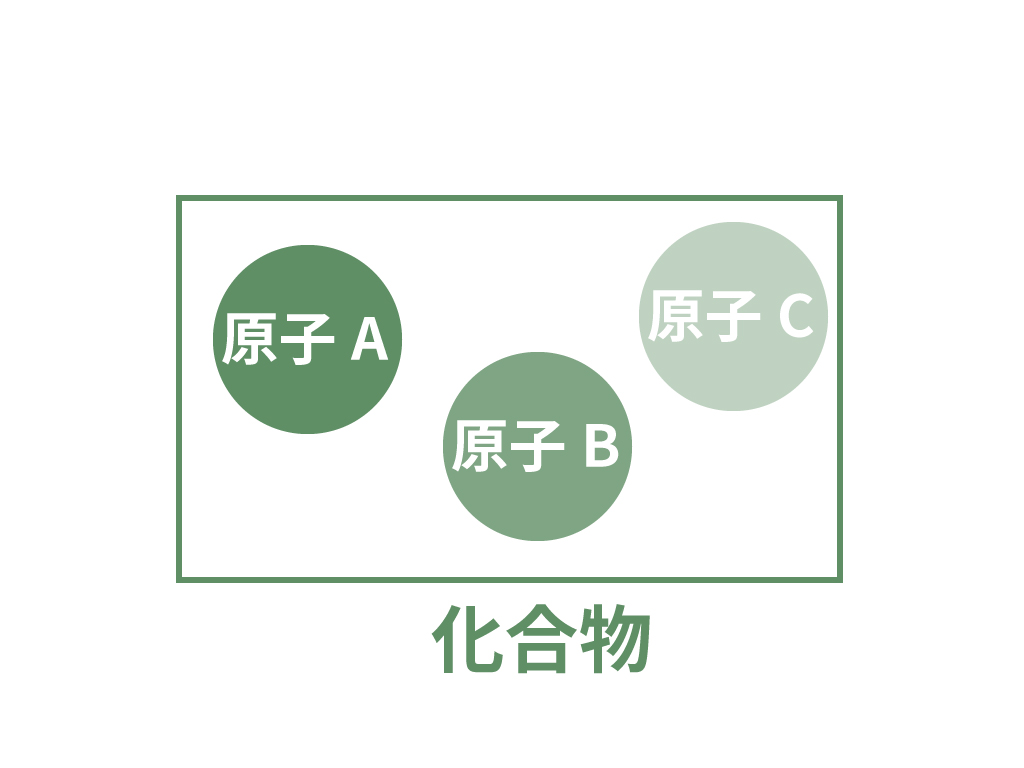
例えば、水とか、二酸化炭素が化合物だね。
化合物は2種類以上の単体に分解できるんだ。
例えば、水は電気分解すると水素と酸素に分解できると実験でわかっている。
水素と酸素は純粋な物質で、しかも1種類の原子から成り立つ「単体」だったよね。
ということは、水は2種類以上の原子からなる化合物なんだよ。
そして、その水の元になっている水素と酸素は、1種類の原子から成り立つ単体ってことね。
うん、以上が単体と化合物と混合物と純粋な物質の違いだよ。
最後にまとめて表で復習しよう。
| 用語 | 意味 |
|---|---|
| 混合物 | 2種類以上の純粋な物質からなる物質 |
| 純粋な物質 | 1種類の物質からなる成り立つ物質 |
| 単体 | 1種類の原子からなる純粋な物質 |
| 化合物 | 2種類以上の単体から成り立つ純粋な物質 |
図であらわすとこうなる。
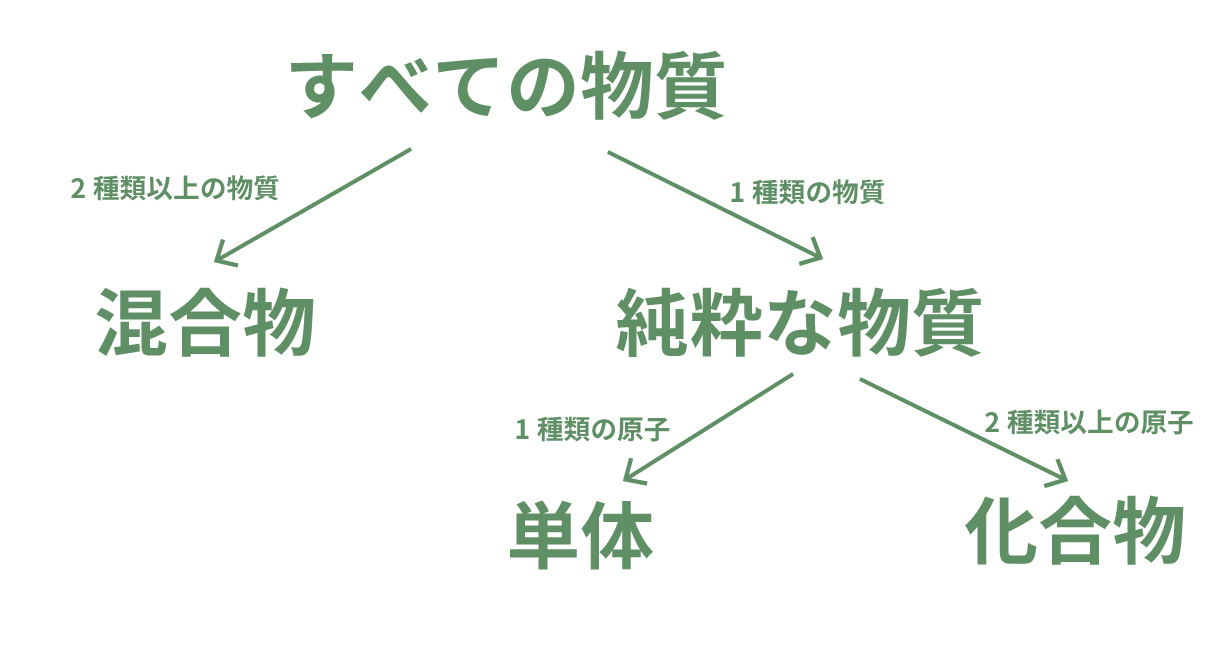

そんじゃねー

ここでは化学式を勉強していこう。
化学式とはズバリ、
ある物質を原子の記号で表したもの
なんだ。
この化学式の書き方は次の2ステップさ。
まずは物質が何の原子でできているか確かめよう。
その原子の記号を調べて、そいつを書けばいいんだ。

例えば、水の化学式を考えてみよう。
水は電気分解すると、
に分かれることが実験で確かめられているね。

だから、
をまずは書いてみよう。

今度はさっき書き出した原子の記号に数字を書いていくよ。

その物質を構成するその原子たちが、一体何個ずつあるのか、という原子の個数を書けばいいんだ。
水の場合は、
という分子のグループ単位で存在している、って「分子とは何か」で勉強してきたよね。
水は「水素の原子2つ」と「酸素の原子1つ」で表せるから、それぞれの原子の数の「2」と「1」をさっきの原子記号「H」と「O」の右下に書けばいいんだね。
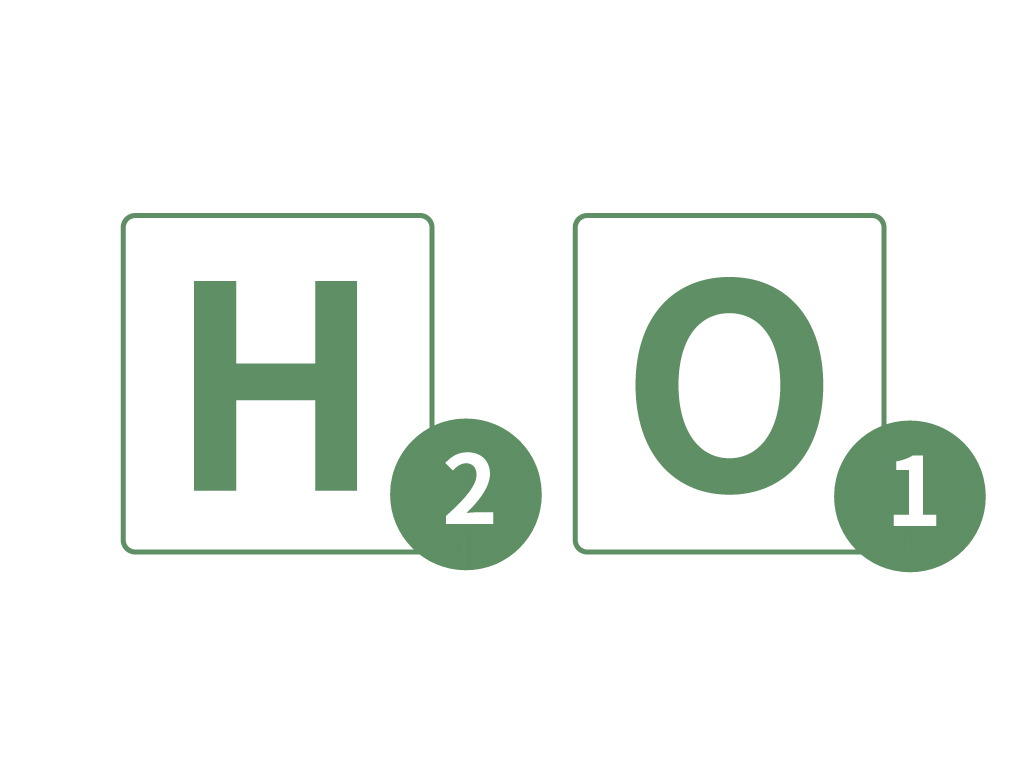
ただし、
1は省略できる!
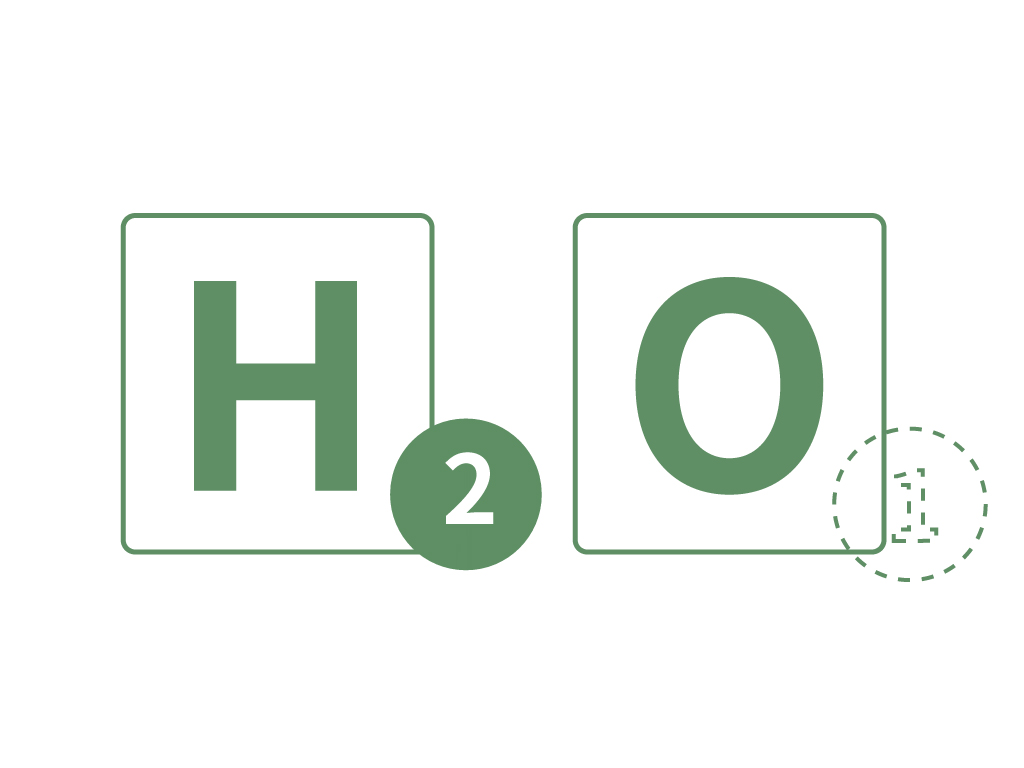
だから、酸素の原子は「$\ce{H2O1}$」ではなくて
$$\ce{H2O}$$
と書くよ。

これで化学式をかけるようになったね。
ふう、って一休みしたいところだけどさ、ちょっと待って。
原子記号の順番
ってどうなってんの??
例えばさっきの水の例。
$$\ce{H2O}$$
$\ce{H}$と$\ce{O}$のどちらの原子を先に書けばいいんだろう!?
よくわかんないから迷っちゃう。
例えば、塩化ナトリウムは、
$$\ce{NaCl}$$
という化学式だ。
でもさ、ナトリウムの原子記号 $\ce{Na}$ が先なんだろう??
別に、$\ce{ClNa}$でもいいじゃないか・・・・と思うよ。
じつは、この、化学式の原子記号の順番にはルールが存在している。
「国際純正・応用化学連合(IUPAC)」という組織が公式文書を発表していて、そのルールをみんな使っているんだ。
公式ルールブックを解読して、原子記号の順番もじっくり学びたいところだけど・・・・・無理!
中2理科の学習範囲では説明できないほど複雑なんだ。
ざっくり大まかにいうと、
金属元素を先に、非金属元素を後に
と覚えておけばいいかな。
さっそく、周期表をチェック。
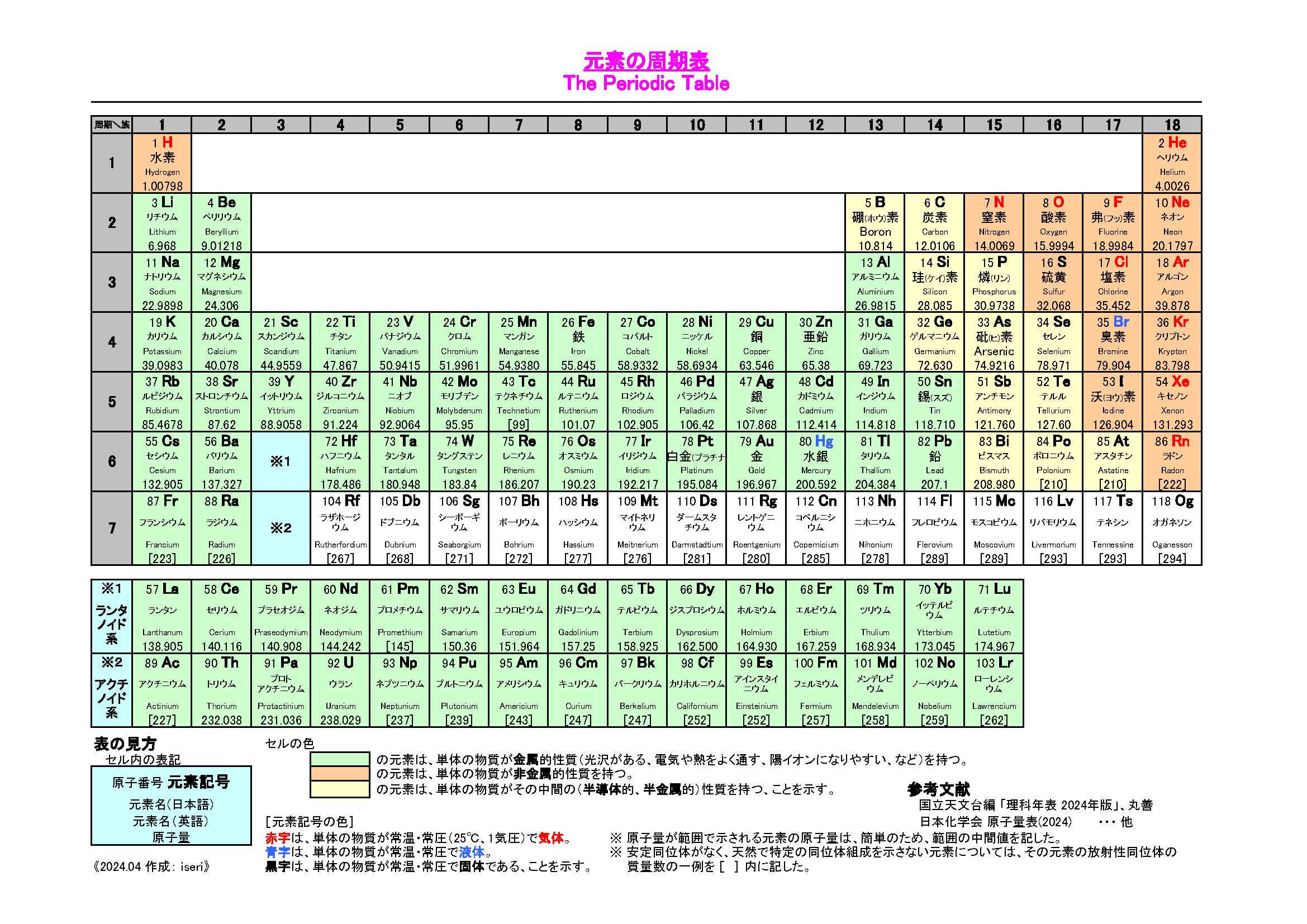
https://www.chiba-kc.ac.jp/user/~iseri/siryo/atom.png より
黄緑が金属元素で、オレンジが非金属元素だ。
だから、もっともっとざっくりいうと、
周期表で左にある原子を先に書いて、右側にある原子はその後にかけばいいんだ。
(ただし水素$\ce{H}$は非金属元素だからのぞく!)
しっくりきたいところだけども、
中2理科の学習段階では「まあ、こういうものか・・・・」と念じるしかない!

次は「単体と化合物と混合物と純粋な物質の違い」を勉強していこう。
そんじゃねー

この前は原子を勉強したきた。
復習しておくと、原子とは、
物質を分解しまくってたどり着くこれ以上小さくできない粒子
だったね。
原子はイギリスのおじさんのドルトンさんが考えたアイディアだったことを思い出そう。

※ イメージだよ
実はそのドルトンさんの原子の発表から8年後の1810年。
今度はイタリアのおじさんの「アボガドロ」さんが、
分子(ぶんし)
というアイディアを発表したんだ。

※ イメージだよ
今日はこの「分子」とは何かをわかりやすく解説していくよ。
ズバリ言ってしまうと、分子とは、
いくつかの原子が組み合わさってできたグループ
なんだ。
アボガドロさんは、
「物質の中身は原子がバラバラに存在してるんじゃない!」
「いくつかの原子が集まった分子というグループを作って、そのグループごとにまとまって物質の中に原子たちが存在している」
と考えたんだ。
例えば「水」を考えてみよう。
水を電気分解すると「酸素」と「水素」に分かれる、と実験で確かめられた。

このことから、水は「酸素」と「水素」の原子で成り立っているんじゃないか、と思うよね。
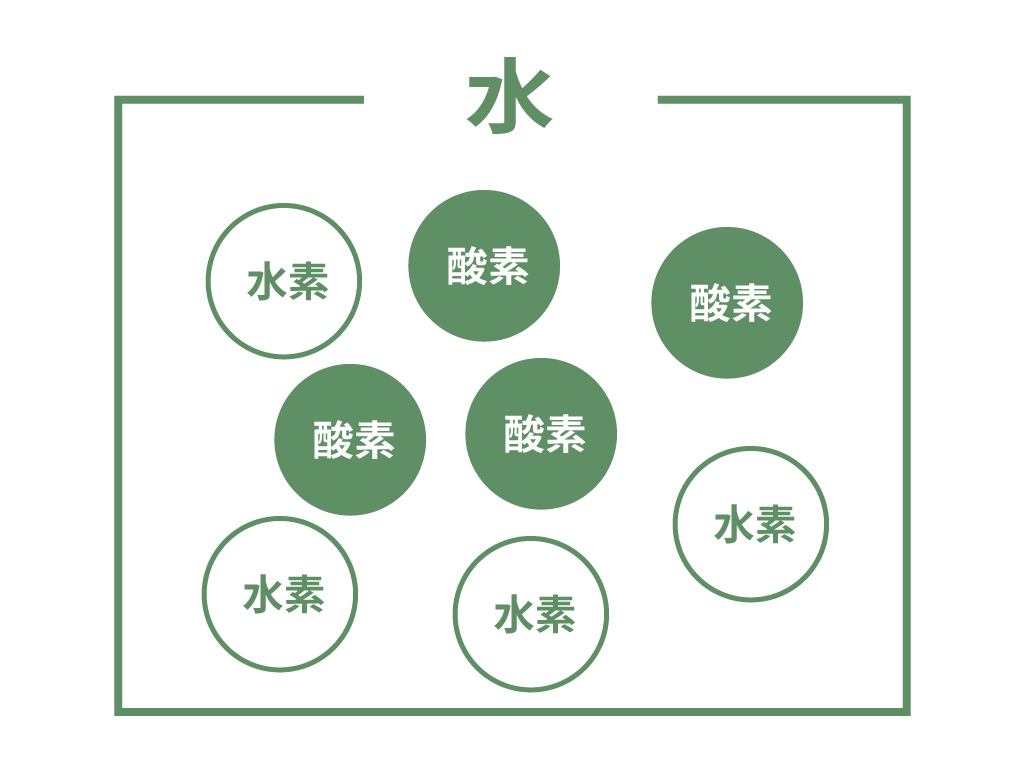
これはドルトンさんの考えだ。
アボガドロさんの発表した「分子」というアイディアは一味違う。
バラバラに水素と酸素の原子が水の中に存在してるんじゃない。
というグループごとにまとまって存在している、と考えたのさ。
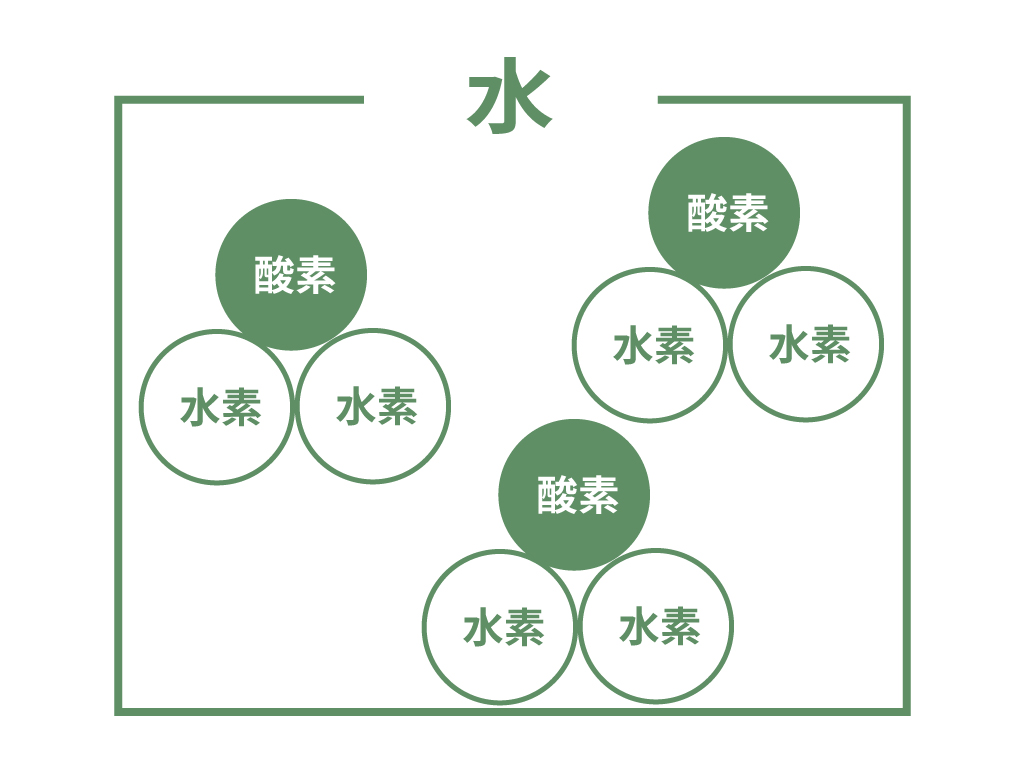
この原子のグループを「分子」と呼んで、この分子が集まって水という物質を作っている、と。

現在の人間界ではこの分子というアイデアが認められているけど、アボガドロさんが発表した直後はそうでもなかったんだよ。
分子を勉強すると、
分子と原子の違いがわからなくなって混乱している子もいるんじゃないかな。
もう一度復習してみよう。
原子は物質を構成するとても小さい粒子。
で、分子はその原子がいくつか組み合わさってできたグループなんだ。

だから、原子は分子の元なわけだね。分子よりも細かい物質の単位が原子。その原子が集まってできたグループの物質の単位が分子というんだ。
まだ原子と分子の違いがしっくりきていない君のために、学校のクラスで例えよう。
君が2年A組の生徒だったとする。
その2年A組というクラスを構成するのは一人ひとりの生徒だよね。
田中さん、高橋さん、鈴木さん・・・・がいるかもしれない。
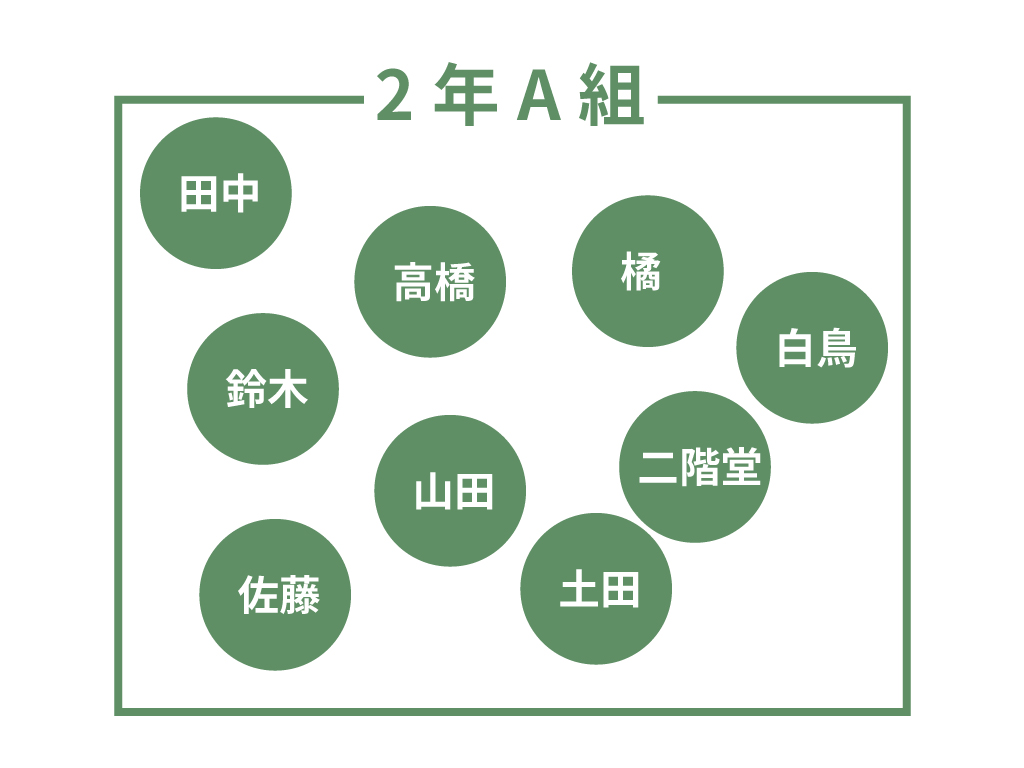
一人一人が集まってできたのが2年A組だ。
原子と分子に例えると、この一人一人が原子に該当するんだね。
でも、1人1人でクラスを考えてみると、バラバラで分かりづらい!
いろんな生徒たちがいるクラス、っていうのはわかるけど、どうもを捉えづらい。
そこで担任の先生は考えた。
「そうだ、班というグループを導入しよう!」
と。
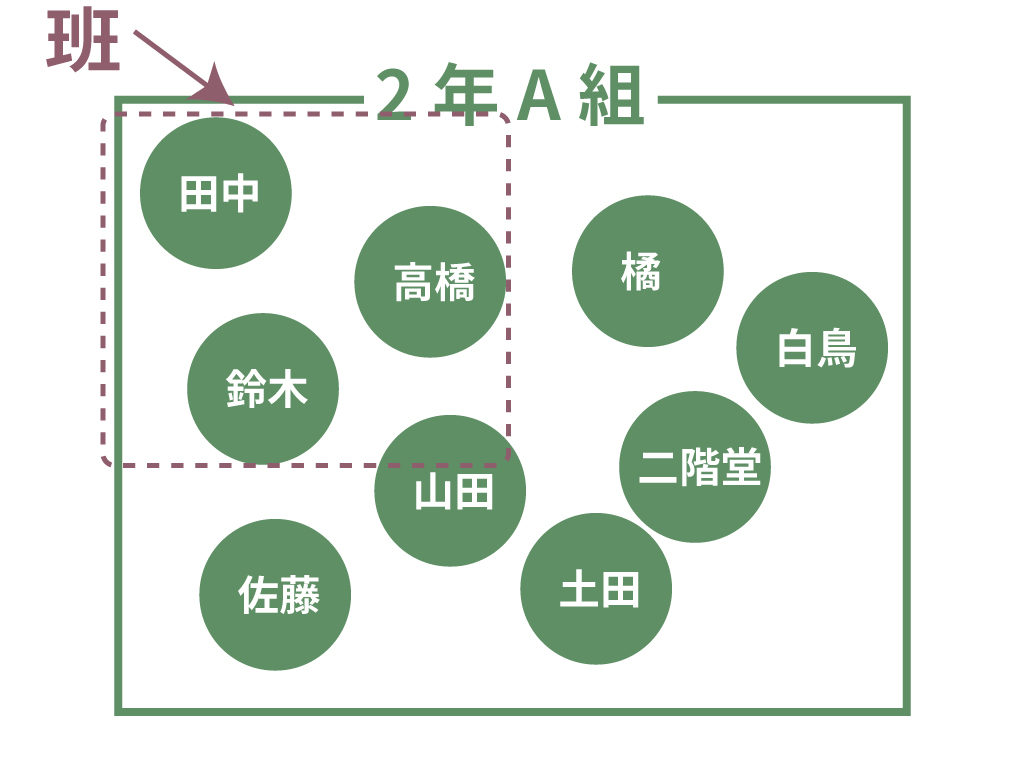
2年A組で「班」というグループをいくつか作ることで、便利になりやしないか。
給食当番、掃除係、日直・・・・といった日々の学園生活を送るための仕事を割り当てやすくなるじゃないか。
とりあえず、田中・高橋・鈴木を「1班」ということにしよう、と。
原子と分子の話でいうと、この先生が思いついた「班」というグループが「分子」に該当するものだよ。
どう?? 原子と分子の違いもしっくりきたかな。
物質を構成するのは原子ってことは間違いない。
だけど、分子(原子がいくつか集まったグループ)で物質を考えた方が説明しやすくなることが多い。
だから、科学の世界では原子だけでなく、分子というアイデアも使うんだ。

そんじゃねー