【図解でわかる】燃料電池の仕組みと化学反応式をわかりやすく解説

おっす!パンダの妖精・月縄だ!
今日は、燃料電池の仕組みについて解説していくぞ。
燃料電池って、ちょっと難しそうに見えるけど、今回はオラがバッチリわかりやすく説明するから安心してな!
今日は、燃料電池の仕組みについて解説していくぞ。
燃料電池って、ちょっと難しそうに見えるけど、今回はオラがバッチリわかりやすく説明するから安心してな!
燃料電池の仕組みをわかりやすく解説!
燃料電池とは、水の電気分解と逆の化学変化を利用する電池だ。
つまり、
水素と酸素が化学変化を起こすときに発生する電気エネルギーを取り出す装置
なんだ。
これってめちゃくちゃエコだよな!
びっくりするけど、この電池から出るのは
水だけ。
地球にやさしいんだ!

燃料電池の仕組みは?
燃料電池って、学校の化学の授業で習った水の電気分解とは逆のことをやってるんだ。
念のために電気分解を復習しておこう。
電気分解とは、
電気エネルギーを使って化学物質を分解する反応のこと
だったよな?
電気分解では、水($ \ce{H2O} $)を電気で分解して、水素($ \ce{H2} $)と酸素($ \ce{O2} $)にする。
逆に燃料電池では、水素と酸素が合わさって水を作るときに電気を生み出すんだよ。
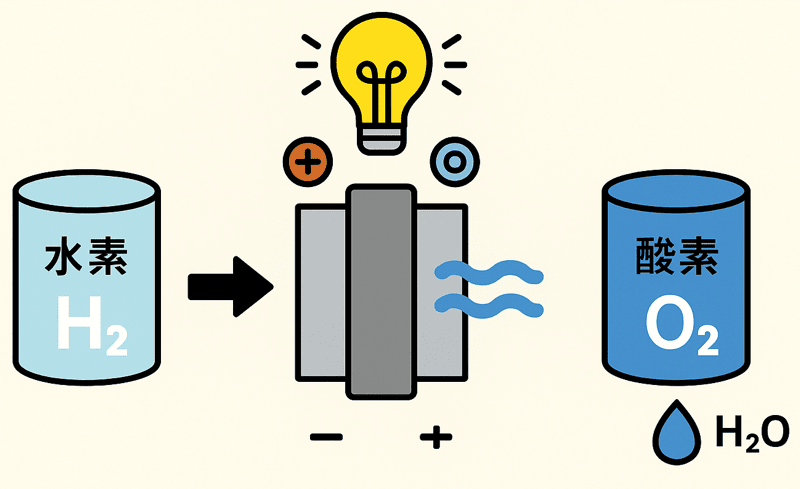
燃料電池の化学反応式
さて、ここで化学大好きなキミのために化学反応式を紹介するぞ。
水素と酸素がくっついて水を作る反応式は、ズバリ、
$$ \ce{2H2 + O2 -> 2H2O + 電気エネルギー} $$
だ。
ツボは、水素と酸素が合体することで電気が生まれるってところさ!
燃料電池の種類 「リン酸型燃料電池」
燃料電池にはいくつかの種類があるんだけど、今回はその中でもリン酸型燃料電池に注目してみよう。
このタイプは、中学校や高校の教科書に登場することが多い形で、高温環境でも使われるんだ。
何よりも、燃料電池は長い時間電流を取り出せるし、有害な物質を発生しないという特徴があるぞ。
まとめ
- 燃料電池の仕組みは、水の電気分解の逆の化学変化を利用する。
- 水素と酸素が合わさって電気エネルギーを生み出し、副産物は「水」だけ!
- リン酸型燃料電池は特にエコで、有害な物質を出さないのが特徴。

燃料電池の仕組み、どうだった?理解できたら未来の科学者も夢じゃない!
エコでクールな技術をマスターして、次の理科の授業で先生をびっくりさせてやろうぜ!
エコでクールな技術をマスターして、次の理科の授業で先生をびっくりさせてやろうぜ!



