【中3理科】電離とは何かわかりやすく解説してみた

おっす、パンダの妖精・月縄だ!
電離(でんり)って聞くと、なんだか難しそうな名前だよな?
でも実は、電離っていうのは、化学の世界では結構シンプルな出来事なんだ!
中学理科の「電離」とはいったい何?
まずは結論から。
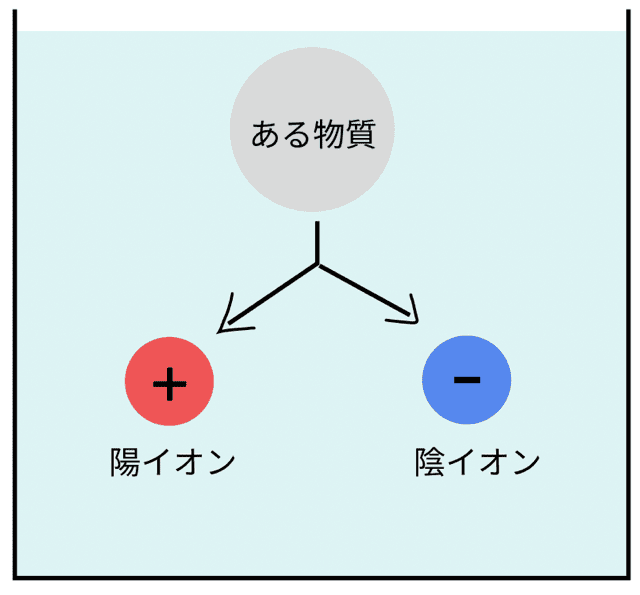
物質が水に溶けて、陽イオンと陰イオンにバラバラに分かれること
これが電離だ!
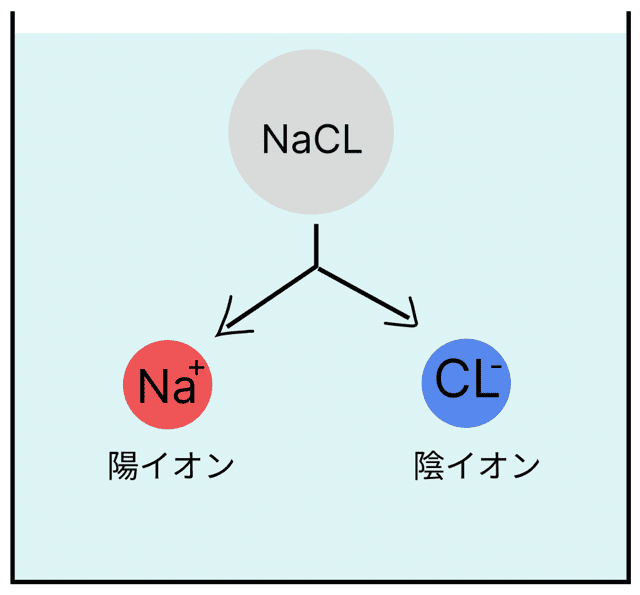
例えば、食塩(塩化ナトリウム)は水に溶けると…
- ナトリウムイオン(Na+)
- 塩化物イオン(Cl−)
この2つに分かれるんだ。
電離はイオン式で表せる!
電離は、イオン式でこんなふうに書けるぞ。
塩化ナトリウム(NaCl)の場合
NaCl → Na+ + Cl−
- NaCl(塩化ナトリウム)
- Na+(ナトリウムイオン)
- Cl−(塩化物イオン)
塩化水素(HCl)の場合
HCl → H+ + Cl−
- HCl(塩化水素)
- H+(水素イオン)
- Cl−(塩化物イオン)
まとめ
- 電離は「水に溶けてイオンに分かれる」こと
- イオン式で電離の様子を表せる

電離って聞くと難しそうだよな。
でも、「水に溶けてイオンになる」ってだけの話なんだぜ!
次は、電解質と非電解質の違いも見ていこうな!



